














Feedback
Please help us to improve this system by providing feedback on your experience with creating this eForm application:
include all your positive and negative experiences as well as what improvements you would like to see in using this
application.
* Is this Application now complete and ready for submission?
Yes
Appendix 1
EForm Name: AE and Bio-Safety Form v3.01
Page:
Section G: Attachments
Section:
Please list all attachments appended in support of this application:
Question:
File Name:
001648 Details of Personnel.pdf

Appendix 2
EForm Name: AE and Bio-Safety Form v3.01
Page:
Section G: Attachments
Section:
Please list all attachments appended in support of this application:
Question:
File Name:
001065 Student Questionnaire summary.pdf
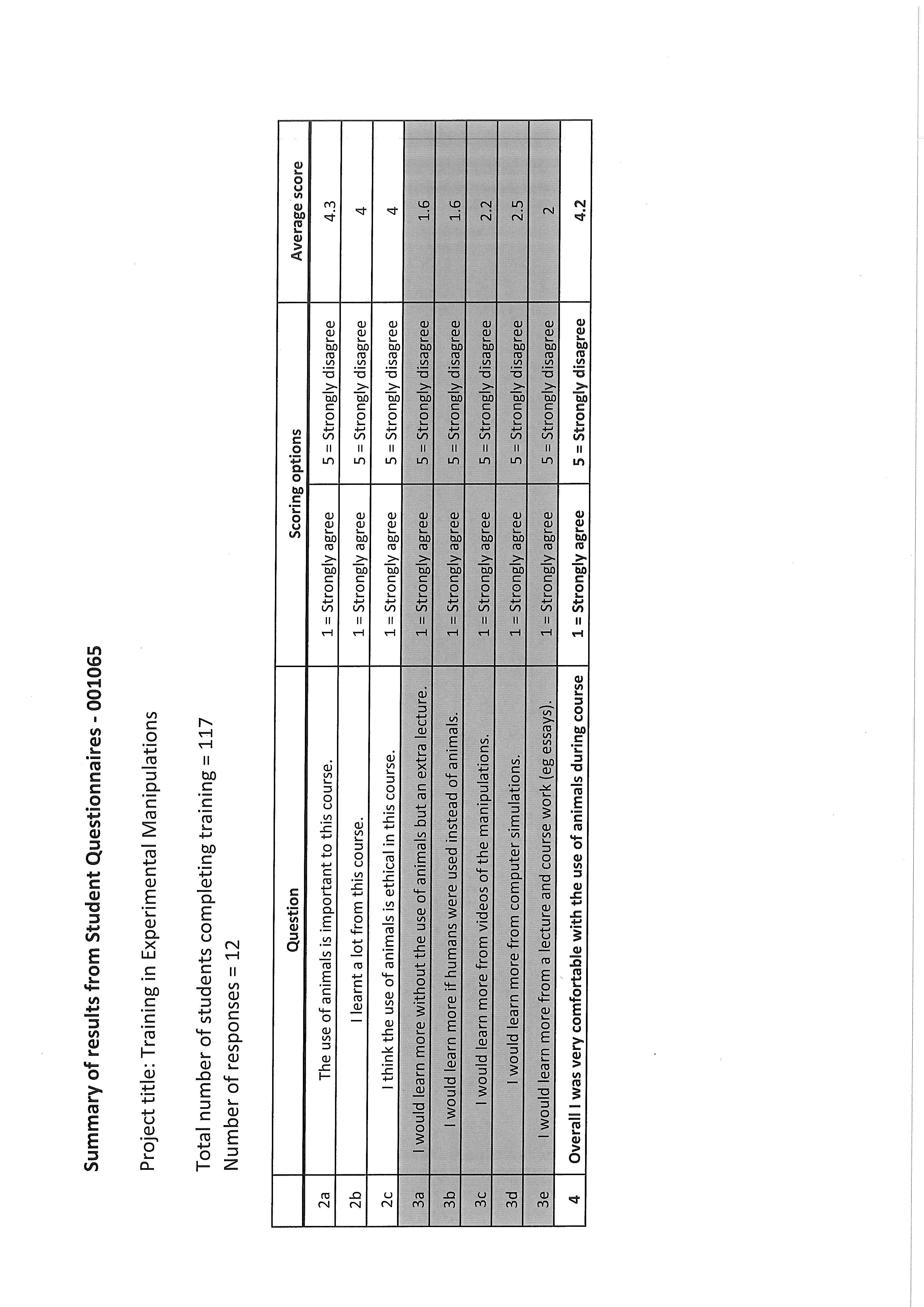
[*]
[1.7]
[1.8]
[1.8]
[4.3]
[4.4]
[3.8]
[3.5]
[3.9]
[1.8]
[*Note that the summary data in the Average Score column is incorrect; the correct average scores have been inserted above]
Appendix 3
EForm Name: AE and Bio-Safety Form v3.01
Page:
Section G: Attachments
Section:
Please list all attachments appended in support of this application:
Question:
File Name:
001065 Student questionnaires.pdf












Appendix 4
EForm Name: AE and Bio-Safety Form v3.01
Page:
Section G: Attachments
Section:
Please list all attachments appended in support of this application:
Question:
File Name:
001648 Manipulations (tracked changes).docx
001648 – Manipulations.
(Manipulation 1)
Euthanasia techniques which may include:
a. Cervical dislocation (mice, rats, birds)
b. Carbon dioxide asphyxiation (mice, rats)
c. Intraperitoneal administration of anaesthetic overdose (mice, rats)
d. Cardiac puncture while terminally unconscious (mice, rats, rabbits)
e. Intravenous administration of anaesthetic overdose (all species)
f. Normal dose of anaesthetic followed by physical method of euthanasia (such as
exsanguination or cervical dislocation) (all species)
a. Its extent and duration. Include time course, Carbon dioxide and anaesthetics take a
dosage etc.
variable time to achieve unconsciousness, up
to half a minute. Anaesthetics will be used as
per IDAO if not administered by a registered
veterinarian. For CO2 – animals will be put into
an empty (of CO2) chamber and it will be filled
at an uncontrolled rate until the animals are
dead.
b. The extent to which the animals may
During the induction phase (with CO2 or
experience pain or distress during or after any
anaesthetics) animals usually experience some
of the manipulations, signs that may be seen
form of distress and show escape behaviours.
and why this is unavoidable
There is also likely to be a stage of anaesthesia
where there is frenzied activity even though
the animal is already unconscious. All training
related to euthanasia will end with death.
c. Detail post manipulation care and/or any
n/a
special housing needs
d. Explain monitoring procedures, humane
Death will be confirmed by observation of
endpoints and contingencies that will be in
physical parameters such as heart rate (none),
place to detect and limit signs of pain or
breathing (stopped), dilated and unreactive
distress.
pupil (in the appropriate species).
(Manipulation 2)
Administration of substances, including oral gavage, intraperitoneal, intramuscular, intravenous ,
inhalation and subcutaneous routes. These are only performed in some species as per Table 1
a. Its extent and duration. Include time course, Administration procedures are usually of less
dosage etc.
than one minute duration. Dosage amounts
will adhere to the maximum administration
volumes from Table 1. Sterile saline will be the
only fluid administered.
b. The extent to which the animals may
Animals may experience transient distress (e.g.
experience pain or distress during or after any
oral gavage) or temporary pain (e.g. at the site
of the manipulations, signs that may be seen
of intravenous or intramuscular injection).
and why this is unavoidable
Subcutaneous injections are administered at
sites with loose skin and don’t seem to cause
more than the most transient (seconds in
duration) pain or distress. Distress may be
seen as wriggling and attempts to escape
restraint, squeaking may be heard from rats
and mice, squealing from guinea pigs. Pain
may be demonstrated by favouring a limb or
imping (where injected in a limb) or paying
ncreased attention (licking, grooming) to the
site of injection.
c. Detail post manipulation care and/or any
Normal care and housing
special housing needs
d. Explain monitoring procedures, humane
Animals will be monitored for the duration of
endpoints and contingencies that will be in
the procedure and a few minutes afterwards
place to detect and limit signs of pain or
as part of the training session. Once animals
distress.
have been returned to cages, they will be
subject to twice daily monitoring by staff as
per normal monitoring procedures. Any
animal that is considered to be still showing
signs of pain or distress (as specified in Table 2)
at the first routine monitoring post procedure
will be given analgesic treatment and
monitored further in consultation with the
Animal Welfare Officer. If the animal fails to
respond to treatment within four hours, it will
be euthanised by CO2 or overdose of
anaesthetic.
Table 1. Administration volumes considered good practice (and possible maximal dose volumes)a
Only the species included in this table will be used to teach administration of substances.
Species
Route and volumes (ml kg-1)
Oral
s.c.
i.p.
i.m.
i.v. (bolus)
i.v. (slow inj.)
Mouse
10 (50)
10 (40)
20 (80)
0.05b (0.1)b
5
-25
Rat
10 (40)
5 (10)
10 (20)
0.1b (0.2)b
5
-20
Rabbit
10 (15)
1 (2)
5 (20)
0.25 (0.5)
2
-10
Sheep
450 (1000)
450 (1000)
N/A
5 (10)
N/A
450 (1000)
Pigeons
5 (20)
2 (4)
N/A
1 (2)
N/A
N/A
aFor non-aqueous injectates, consideration must be given to time of absorption before re-dosing. No
more than two intramuscular sites should be used per day.
Subcutaneous sites should be limited to two or three sites per day. The subcutaneous site does
not include Freund’s adjuvant administration.
bValues in millilitres per site.
(Diehl et al, “A Good Practice Guide to the Administration of Substances and Removal of Blood, Including
Routes and Volumes”).
Table 2. Monitoring criteria for animals following administration of substances
Species
Criteria
Mouse
Activity
Posture
Coat
Respiration
Dehydration
CNS signs
Rat
Activity
Posture
Coat
Respiration
Dehydration
CNS signs
Rabbit
Activity
Respiration
Dehydration
CNS signs
Ear position
Sheep
Activity
Respiration
Posture
Appetite
Bruxism
Pigeon
Behaviour
Grooming
Aggression
(Manipulation 3)
Anaesthesia techniques, including induction by inhalation (mice and rats) or by injection (all
species), maintenance of gaseous anaesthesia (mice, rats, sheep), monitoring of reflexes and
inhalation and injectable delivery of drugs, reflex monitoring, adjustment of anaesthetic depth.
a. Its extent and duration. Include time
Extent and duration of anaesthesia will be
course, dosage etc.
dependent on the type of anaesthetic being
used. This can vary widely from several
minutes through to several hours. Routine
teaching will most regularly use an inhalation
anaesthetic (isoflurane) of short duration (e.g.
10-20 minutes to show induction,
establishment on face mask and then
adjustment of anaesthetic levels with
demonstration of reflexes after changes) or
injectable anaesthetic such as
ketamine/domitor which has a much longer
duration (up to 1 hour sleep time) and possibly
use of a reversal agent.
b. The extent to which the animals may
Pain is unlikely and is not a large feature of
experience pain or distress during or after any anaesthetics, although minor needle stick pain
of the manipulations, signs that may be seen
may be involved at the site of administration
and why this is unavoidable
of injectable anaesthetics. Brief distress (less
than a minute) and confusion is likely on
induction of any anaesthesia. Recovery from
anaesthesia is also likely to produce some
confusion, possibly distress, for the duration of
‘hang over’ (metabolism) from the drugs that
were used. For inhalation anaesthetics that
are largely breathed out rather than
metabolised then recovery to a normal state is
much quicker than recovery from injectables
which do need to be metabolised through the
liver. Animals recovering from injectables may
be affected for hours after regaining
consciousness and may be quiet, huddle, eat
and drink less than normal and be slow to
move if a handler puts their hand in the cage.
c. Detail post manipulation care and/or any
The previous application had all anaesthetic
special housing needs
procedures as terminal, but I believe that
recovery from solely an anaesthetic is justified
to teach the signs of post-anaesthetic
behaviour and care. Any animals which have
had surgery under anaesthesia will be terminal
at the end of the procedure without regaining
consciousness.
d. Explain monitoring procedures, humane
Animals will be monitored continuously during
endpoints and contingencies that will be in
the period of pre-anaesthetic assessment,
place to detect and limit signs of pain or
induction and maintenance of anaesthesia and
distress.
recovery of consciousness. Once animals
have recovered consciousness and are able to
stand, they will either be monitored
intermittentlyhourly for the remainder of the
working day (as per Table 2) or euthanised
(dependsing on the aim of the teaching
session). Animals will be euthanised by the
end of the working day on which they are
anaesthetised.
(Manipulation 4)
Blood collection techniques, which may include tail tip, tail vein, saphenous vein, mandibular vein,
jugular vein, cardiac puncture and ear vein as appropriate to the species.
a. Its extent and duration. Include time
Rats, mice, guinea pig and rabbit only
course, dosage etc.
Blood collection techniques take a variable
but short period of time (minutes). All
procedures will be taught as per current good
practice including only teaching appropriate
techniques for each species and taking no
more than the safe single bleeding volume if
the animal is to remain alive at the end of the
procedure.
This equates to no more than
Mouse, rabbit and guinea pig 7.7 mL/Kg
Rat 5.5 mL/Kg
Sheep 10 mL
b. The extent to which the animals may
No animal will be subjected to more than one
experience pain or distress during or after any blood collection procedure, to minimise blood
of the manipulations, signs that may be seen
loss and distress. All animals will be
and why this is unavoidable
restrained during procedures so the main
signs seen will be attempts to escape (which is
normal for any blood collection procedure)
and vocalisation in some species (squeaks,
squeals). Cardiac puncture will only be taught
as a terminal procedure under anaesthetic or
immediately after death due to another
means such as CO2 asphyxiation.
c. Detail post manipulation care and/or any
Post manipulation care will include pressure
special housing needs
at the site of blood collection where
appropriate and frequent monitoring until
sure that there is no further bleeding at the
site of collection. Blood clotting at the site of
collection usually takes less than 2 minutes
but observation will continue uninterrupted
until bleeding has stopped.
d. Explain monitoring procedures, humane
Periodic checks will occur throughout the rest
endpoints and contingencies that will be in
of the working day for those animals that are
place to detect and limit signs of pain or
to survive. The Uusual daily monitoring will
distress.
recommence on the day after the procedure.
Animals will not be bled again for at least two
weeks.
(Manipulation 5)
Handling and sexing of animals.
a. Its extent and duration. Include time course, An eEstablished training modules exists for
dosage etc.
teaching handling, sexing and euthanasia of
rats, mice, guinea pigs, rabbits, birds and
birdsand sheep.
b. The extent to which the animals may
No pain results from these procedures,
experience pain or distress during or after any though the animals may exhibit signs of
of the manipulations, signs that may be seen
stress. This is unavoidable during the teaching
and why this is unavoidable
until the students are competent and
confident.
c. Detail post manipulation care and/or any
None required.
special housing needs
d. Explain monitoring procedures, humane
N/A
endpoints and contingencies that will be in
place to detect and limit signs of pain or
distress.
(Manipulation 6)
Surgical techniques which may include suture placement, laparotomy (opening the abdomen),
subcutaneous implantation, vascular access port placement, implantation of indwelling catheters.
These procedures will be taught on terminally anaesthetised patientsrats, mice and sheep.
Students must be proficient in the anaesthetic techniques prior to commencing surgical training
on live anaesthetised animals. They must also have practiced on cadavers prior to training on
anaesthetised patientsanimals.
a. Its extent and duration. Include time
These procedures will take a variable amount
course, dosage etc.
of time, but will only occur on terminally
anaesthetised animals.
b. The extent to which the animals may
Pain or distress may be experienced on
experience pain or distress during or after any induction of anaesthesia as per 2.4.3
of the manipulations, signs that may be seen
and why this is unavoidable
c. Detail post manipulation care and/or any
All animals will be killed at the end of teaching
special housing needs
without recovery from a surgical depth of
anaesthesia
d. Explain monitoring procedures, humane
Routine anaesthetic monitoring such as
endpoints and contingencies that will be in
breathing, heart rate and reflexes will occurbe
place to detect and limit signs of pain or
carried out as appropriate to the species.
distress.
Appendix 5
EForm Name: AE and Bio-Safety Form v3.01
Page:
Section G: Attachments
Section:
Please list all attachments appended in support of this application:
Question:
File Name:
Memo to the AEC 001648.docx
Memo to the Animal Ethics Committee
Subject: Letter of conditional approval of 001648
From:
Responsible Investigator
I. Given that some of the animals will be handled, injected, sampled from and then returned
to their cages, details should be given for some of the answers which are currently N/A, such
as D4c-h. Information given in the supplemental document don’t include monitoring criteria
for animals recovering from anaesthesia, sampling etc, and clear humane endpoints.
Reference is made to standard monitoring and intermittent monitoring, but this is insufficient.
I have amended the document “001648 – Manipulations” to include more details of
monitoring procedures and end points where appropriate. I’ve also added a second table –
“Table 2. Monitoring criteria for animals following administration of substances”.
II. Some manipulation endpoints state that if any pain or distress is observed, the animals
will be killed.
Are there no other options to improve outcomes other than death?
I’ve included the statement “Any animal that is considered to be showing signs of pain or
distress (as specified in Table 2) will be given analgesic treatment and monitored further in
consultation with the Animal Welfare Officer. If the animal fails to respond to treatment
within four hours, it will be euthanised by CO2 or overdose of anaesthetic”.
III. In the supplemental information, animals are referred to as patients, e.g. manipulation 6.
This word should be replaced with animal.
Sorted.
IV. Is there value in expanding table one to include all the animals being manipulated?
I’ve extended Table 1 to include sheep and pigeons.
V. It is not clear from the descriptions which manipulations relate to sheep and why some of
the manipulations are limited to only some species.
I’ve indicated, under each manipulation, which items are applicable to which species.
VI. How are researchers notified of available tissues or blood etc?
The facility managers in the
are the
personnel doing the training. They are generally well aware of any other researchers that are
looking for tissues, and so inform them when they become available. There is nowhere in the
application form to add this information.
VII. There are no clear guidelines for monitoring the animals that return to their cages- as we
would expect from research staff, and no clear humane endpoints.
I’ve addressed this in the amended application.






























