Methamphetamine: History,
Pathophysiology, Adverse Health
Effects, Current Trends, and Hazards
Associated with the Clandestine
Manufacture of Methamphetamine
David Vearrier, MD,
Michael I. Greenberg, MD, MPH,
Susan Ney Miller, MD, Jolene T. Okaneku, MD, and
David A. Haggerty, MD
Introduction
Developed as an amphetamine derivative, methamphetamine quickly
became a popular medication during the 1940s and 1950s, prescribed for
a variety of indications. Extensive diversion of methamphetamine during
the 1960s and an increasing awareness of the adverse health effects
associated with methamphetamine led to the withdrawal of most of the
indications for licit methamphetamine use and declines in legal produc-
tion of the drug. However, the illicit manufacture of methamphetamine
increased to meet the demand for methamphetamine, and methamphet-
amine abuse has increased with variable geographic penetrance over the
last 30 years.
Methamphetamine is an indirect sympathomimetic agent that is distin-
guished from amphetamine by a more rapid distribution into the central
nervous system (CNS), resulting in the rapid onset of euphoria that is the
desired effect for those abusing the drug. Increases in monoamine
neurotransmission are responsible for the desired effects—wakefulness,
energy, sense of well-being, and euphoria—as well as the excess
sympathetic tone that mediates many its adverse health effects.
Methamphetamine is associated with adverse effects to every organ
system. Although the most significant morbidity and mortality occur
because of cardiovascular effects, such as myocardial infarction and
hypertensive crisis, no organ system remains unscathed by methamphet-
Dis Mon 2012;58:38-89
0011-5029/2012 $36.00 ⫹ 0
doi:10.1016/j.disamonth.2011.09.004
38
DM, February 2012
link to page 38
amine abuse. Methamphetamine abuse is a serious public health problem
because of both costs associated with treatment of methamphetamine-
associated adverse health effects and crime and violence perpetrated to
obtain methamphetamine or because of methamphetamine-related aggres-
sive behavior.
Of further concern are the hazards and environmental effects of “meth
labs,” frequently small operations housed in residential buildings, where
methamphetamine is manufactured from precursor chemicals. Hazards
associated with methamphetamine laboratories include blast injuries,
thermal burns, chemical injury, and toxic exposures. Unfortunately, a
significant percentage of methamphetamine laboratories are housed in
residential buildings where children are present, potentially resulting in
pediatric exposures to methamphetamine, precursor chemicals, and drug
use paraphernalia.
This article reviews the history of methamphetamine use and abuse,
describes its mechanism of action and pathophysiology, delineates
adverse health effects, and describes current epidemiologic trends. It also
discusses the process and precursor chemicals involved in the manufac-
ture of methamphetamine and hazards associated with clandestine meth-
amphetamine laboratories.
The History of Methamphetamine
Discovery and Early Methamphetamine Use
Amphetamine-type stimulants, which include methamphetamine and
amphetamine, were developed as synthetic alternatives to ephedra.
Ephedra is a botanic extract of
Ephedra sinica and has been used in
traditional Chinese medicine as ma huang for over 5000 years. In 1885,
ephedrine, the active alkaloid present in ephedra, was extracted and
studied. Ephedrine was recognized to be similar to epinephrine, which
was also isolated around the turn of the 20th century, but could be taken
orally, had a longer duration of action, produced more pronounced and
dependable CNS stimulation, and had a larger therapeutic index. The
search for a synthetic ephedrine substitute resulted in the development of
amphetamine-type stimulants, produced via modification of the ephedrine
skeleton with the pharmaceutical goals of CNS stimulation, bronchodi-
lation, or nasal
vasoconstriction.1-3 Japanese chemist Akira Ogata first
synthesized methamphetamine in 1919 using ephedrine as a precursor.
Early amphetamine use was primarily via nasal insufflation. In 1932,
Smith, Kline, and French began marketing the amphetamine inhaler
Benzedrine for use in asthma and congestion. The insufflated amphet-
DM, February 2012
39
link to page 38 link to page 38 link to page 38 link to page 38 link to page 38 link to page 38
amine caused vasoconstriction of the nasal mucosa, decreasing mucosal
swelling and edema, and the inhaler was initially available without a
prescription. In 1959 the S. Pfeiffer Company began producing Valo
inhalers that contained 150-200 mg of
methamphetamine.4,5
The Heyday of Licit Methamphetamine Use
Desirable “side effects” associated with amphetamine-type stimulant
inhalers were noted, resulting in expanding indications for amphetamines
and the introduction of oral amphetamine-type stimulant medications. For
example, the side effect of wakefulness suggested its value in treating
narcolepsy and conditions of drowsiness or exhaustion. Its appetite-
depressant effects led to the use of amphetamines, including metham-
phetamine, for weight
loss.4 Other early indications and off-label uses for
methamphetamine included schizophrenia, asthma, morphine addiction,
barbiturate intoxication and narcosis, alcoholism, excessive anesthesia
administration, migraine, heart block, myasthenia gravis, myotonia,
enuresis, dysmenorrhea, Meniere’s disease, colic, head injuries, hypoten-
sion, seasickness, persistent hiccups, heart block, head injuries, infantile
cerebral palsy, codeine addiction, tobacco smoking, pediatric behavior
issues, Parkinson’s disease, and
epilepsy.5 Amphetamines and their
analogs were being presumptively promoted as effective and safe without
risk of addiction. In 1940, methamphetamine tablets under the commer-
cial name Methedrine were introduced to the market by the Burroughs
Wellcome
Company.1,6
Methamphetamine was also used by the military. In World War II,
methamphetamine was available to military personnel as Pervitin in
Germany and Philopon in Japan. Temmler Pharmaceutical Company
introduced Pervitin in 1938 to the European market. Pervitin was
available as 3 mg tablets that physicians could provide for the German
military units. Dainippon Pharmaceutical Company made Philopon avail-
able in Japan in 1941. Methamphetamine in Germany and Japan and
amphetamine use in the USA were used to increase alertness, reduce
fatigue, and suppress the appetite of
soldiers.4,5 Use of methamphetamine
extended to include war-related industry workers to improve shift work
abilities. Later, the USA military used amphetamines in the Korean War
and the Vietnam War. Today, the use of stimulants, like amphetamines
and methamphetamine, is permitted to treat combat fatigue and promote
wakefulness in combat. A survey of Persian Gulf War pilots reported
substantial use of stimulants to decrease fatigue during
combat.1
During the 1940s and 1950s, methamphetamine was liberally prescribed
for numerous indications and large quantities of it were licitly produced.
40
DM, February 2012
link to page 38 link to page 38 link to page 38 link to page 38 link to page 38
A broad segment of the population used methamphetamine for a variety
of reasons. Housewives, truck drivers, students, and professionals used
amphetamines and methamphetamine to promote wakefulness, improve
mood or attention, and lose weight. Numerous users gradually increased
the doses they used as they developed tolerance to the effects of the
drugs.1,4,5
The ways in which the medications could be misused spread quickly.
Inhalers could be broken open and the contents ingested directly or filters
could be soaked in alcohol or coffee to reduce irritation of the mouth.
Extracting drugs from inhalers for intravenous injection was another
method of abuse, first being reported in 1959. Reports of robberies,
murder, and other violent acts were linked to inhaler
misuse.4,5 Prison
populations also abused these inhalers, which could be smuggled within
containers or letters. Methamphetamine abusers would combine the drug
with illicit substances, such as heroin or barbiturates. Use in conjunction
with a barbiturate produced what was referred to as “bolt and jolt,” a
street term for the increased pleasure associated with this combination of
drugs.1,4,5
In response to a Food and Drug Administration warning of misappli-
cation of the inhalers, some pharmaceutical companies responded by
adding a denaturant to deter ingestion. Abusers adapted by injecting the
product after boiling off the denaturant. In 1959, the Food and Drug
Administration restricted amphetamine and dextroamphetamine inhalers
to prescription-only distribution. Methamphetamine inhalers, such as
Valo, continued to be marketed until 1965. Starting with Benzedrine in
1949, most of these nasal inhalers were removed from the market by
1971.4
The Gradual Recognition of Adverse Health Effects
Reports of serious adverse health effects of amphetamines began
appearing as early as 1935. One early study reported that even at the
recommended therapeutic dose of an amphetamine inhaler, most subjects
experienced pallor, flushing, palpitations, and increases in pulse rate and
blood pressure. Six of the 20 subjects in that study developed multiple
extrasystoles and chest pain. Other studies reported convulsions, coma,
loss of consciousness, nausea, vomiting, difficulty breathing, tremor,
tetany, tachycardia, pallor, psychosis, and
cyanosis.4,5
As an early response to recognition of potential dangers associated with
amphetamine use and misuse, state and federal restrictions were enacted,
halting the over-the-counter sale of oral amphetamine preparations. These
restrictions required that amphetamines be marketed under a label
DM, February 2012
41
link to page 38 link to page 5 link to page 38
TABLE 1. Street names for methamphetamine
Meth
Dimethylphenethylamine
Speed
Methedrine
Crystal meth
Desoxyn
Ice
Chalk
Batu
Poor man’s cocaine
Shabu
Tweak
Glass
Uppers
Tina
Biker’s coffee
Crank
Trash
Go-fast
Black beauties
Stove top
Methlies quick
Yaba
Yellow barn
warning against use except under medical supervision. However, inhalers
containing amphetamines or methamphetamine were not covered under
this
regulation.4
As the abuse of methamphetamine increased, so did the number of
monikers associated with the drug
(Table 1). During the 1960s, the term
“speed freaks” became popular to describe high-dose, compulsive users
of amphetamine and methamphetamine.
1,5 Demographically, amphet-
amine-type stimulant abuse at that time was most common among
Caucasians with a middle-class socioeconomic status. The prevention
slogan “speed kills” was introduced by antidrug activists during the
1960s, prompted by the serious medical and psychiatric consequences of
abuse, although some argue that the slogan may have done as much to
popularize the abuse of amphetamines as to prevent it.
In response to the burgeoning diversion of legally produced amphet-
amine-type stimulants to the criminal underworld, the USA federal
government passed the Drug Abuse Control Amendments of 1965, which
required record keeping throughout the manufacture, distribution, pre-
scription, and sale of these medications. Ultimately, this bill was
ineffective in preventing diversion of amphetamine-type stimulants to the
black market. Subsequently, the Comprehensive Drug Abuse Prevention
and Control Act of 1970 limited the accepted medical uses for prescribed
amphetamines and classified amphetamines as Schedule II medications.
Over the course of the 1970s, there was a gradual decrease in the number
of amphetamines prescribed and decreasing legal production of the drugs
was resulting in less diversion to the street. A 90% decrease from
prelegislation level was accomplished by the mid-1980s; the rate at which
amphetamines was being prescribed had decreased by 90% from the
42
DM, February 2012
link to page 38 link to page 38 link to page 38 link to page 38 link to page 38 link to page 38 link to page 38
heyday of the 1960s and continued to decrease by another one-third by
1990.1
Diversion of Pharmaceutical Products and Illicit
Manufacture
It has been estimated that legal pharmaceutical production of amphet-
amine was 3.5 billion tablets in 1958, enough to supply every person in
the USA at the time with 20 standard
doses.4 Prescriptions peaked in 1967
at 31 million, whereas amphetamine production increased to 10 billion
tablets by
1970.7 A consequence of the overproduction of amphetamines
was diversion to illegal traffic. Supplies of amphetamine and metham-
phetamine from legal production found their way to the black market via
pharmaceutical companies, wholesalers, pharmacists, and
physicians.4,6
Illegal manufacture of methamphetamine emerged as a new source of
the drug and became increasingly important as a diversion of licitly
produced methamphetamine became more difficult. The first known illicit
production of methamphetamine occurred in 1962 in San Francisco, CA.
During the late 1960s, the Haight-Ashbury neighborhood of San Fran-
cisco became a center of methamphetamine abuse, particularly among
young adults and college students. Illegal manufacture was imperfect and
the methamphetamine contained substantial amounts of impurities. How-
ever, by the mid-1980s, virtually all street methamphetamine was
manufactured in clandestine laboratories rather than diverted from legally
produced pharmaceutical
products.5,7,8
Association with motorcycle gangs led to the early reputation of
methamphetamine as a “biker drug” in the 1960s and 1970s. The
nickname “crank” originated from the bikers’ tendency to transport the
methamphetamine in the crankcases of their motorcycles. Motorcycle
gangs, including Hell’s Angels, were responsible for manufacturing and
distributing methamphetamine along the Pacific Coast and have been
associated with distribution networks that contributed to a rise in
methamphetamine use in the 1960s. These motorcycle gangs contributed
up to 90% of methamphetamine produced in the USA in the 1970s and
1980s. Their customer base was primarily in Southern California and
Oregon and much of the distribution involved the intravenous or
crushable tablet
form.1 Eventually, as illicit production of methamphet-
amine shifted to Mexico, the motorcycle gangs transitioned to purchasing
methamphetamine from Mexican manufacturers and focused their profit-
making on the distribution of the
drug.1,7
Following a lull in amphetamine and methamphetamine use during the
1970s and early 1980s because of declining prescriptions and licit
DM, February 2012
43
link to page 38 link to page 38 link to page 7 link to page 38
TABLE 2. Selected methods of self-administration of methamphetamine
Method of
Slang Terms Associated
Administration
with Technique
Anal suppository
Butt rocket, plugging
Ingestion
None
Inhalation
Chasing the white dragon
Insufflation
Snorting
Intravenous injection
Banging, mainlining, slamming
Vaginal suppository
None
production, methamphetamine use in the West Coast began to increase
again in the mid-1980s and steadily spread into the Midwest through the
1990s. The Northeast and Mid Atlantic were relatively spared up until just
this past
decade.1 Epidemiologically, methamphetamine abuse in the
1980s occurred predominantly among Caucasian males, many of whom
were truck drivers, construction workers, and other blue-collar workers.
During this period, a new form of methamphetamine, methamphet-
amine hydrochloride, was popularized. “Ice” or “crystal meth,” as
methamphetamine hydrochloride was called, could be smoked, resulting
in an almost immediate onset of euphoria and contributing to its
increasing popularity among amphetamine abusers. The epidemic started
in West Honolulu and included those from the working class, public
housing projects, and Filipino community, but over time expanded to
Hawaii and the West Coast and then throughout the
USA.7,8 Table 2
describes some of the more popular methods of methamphetamine
self-administration. More legislation was passed during this period, which
included the Federal Controlled Substance Analogue Enforcement Act of
1986 and Chemical Diversion and Trafficking Act of 1988, with the latter
act regulating precursor chemicals in an attempt to stem the illicit
production of
methamphetamine.2
The 1990s experienced an expansion of local manufacture and regional
distribution of methamphetamine. Manufacturing in both “mom-and-pop
labs” and large-scale “super labs” became widespread throughout the West
Coast and Midwest states. In areas with adequate illicit drug infrastructure
and high methamphetamine demand, like the Central Valley of California,
organized networks of producers and distributers predominate. In areas with
less established infrastructure, the methamphetamine supply is produced by
local “cooks” and distributed by a relational network of people. Clandestine
laboratories are often, although not exclusively, set up in rural areas because
of the strong odors associated with methamphetamine production and are
moved frequently to prevent detection.
44
DM, February 2012
link to page 38 link to page 38 link to page 38 link to page 9 link to page 38 link to page 38 link to page 38
In response to an epidemic of methamphetamine abuse, the federal
government has passed measures designed to stem rising methamphet-
amine manufacture and abuse. The Methamphetamine Control Act of
1996 was passed to strengthen penalties and tighten controls on precur-
sors.7,8 The most recent federal law is the Combat Methamphetamine
Epidemic Act of 2005, which regulates the purchase of products contain-
ing pseudoephedrine, ephedrine, and phenylpropanolamine, all of which
can be used in the manufacture of methamphetamine. Specifically, drugs
containing these precursors must be stored behind a pharmacy counter;
purchase requires proof of identification, and purchases are limited to a
maximum of 3.6 g of pseudoephedrine per
day.1 Despite this recent law,
methamphetamine manufacturers circumvent these restrictions by
“smurfing” or sending multiple people to make several pseudoephedrine
purchases at different retail centers.
Currently, most of the methamphetamine available in the USA is
produced domestically or in Mexico. Since the early 1980s, Mexican drug
cartels have trafficked both methamphetamine and its precursors into the
USA. Cartels in Mexico purchase bulk ephedrine or pseudoephedrine
from countries with less strict oversight of methamphetamine precursor
chemicals, such as India, Germany, and China. Despite efforts by both the
USA and the Mexican governments to prohibit the import of precursor
chemicals, methamphetamine production continues to
increase.1,8
Pathophysiology
Methamphetamine is a member of the phenylethylamine class of
psychostimulants. Similar in structure to amphetamine, an added N-
methyl group confers added lipid solubility, allowing for more rapid
crossing of the blood– brain barrier
(Fig 1). This property of metham-
phetamine causes a higher ratio of central to peripheral action and a more
rapid onset of central
effects.9 The pathophysiology of methamphetamine
primarily relates to its effects on multiple neurotransmitter systems.
Dopamine (DA), a catecholamine, is the major neurotransmitter impacted
by methamphetamine use. However, methamphetamine also affects
serotonergic, noradrenergic, and glutamatergic systems as
well.10 The
acute adverse effects of such neurotransmitter dysregulation are predom-
inantly because of catecholamine excess. Specifically, this involves
cardiovascular activation via norepinephrine release from sympathetic
nerve endings as well as psychoactive stimulation from large quantities of
DA release into brain synapses, including the caudate, putamen, and
ventral striatal
regions.11,12 In contrast, chronic methamphetamine use
has been shown to cause persistent dopaminergic deficits.
DM, February 2012
45
link to page 10 link to page 38 link to page 39 link to page 39 link to page 39 link to page 39
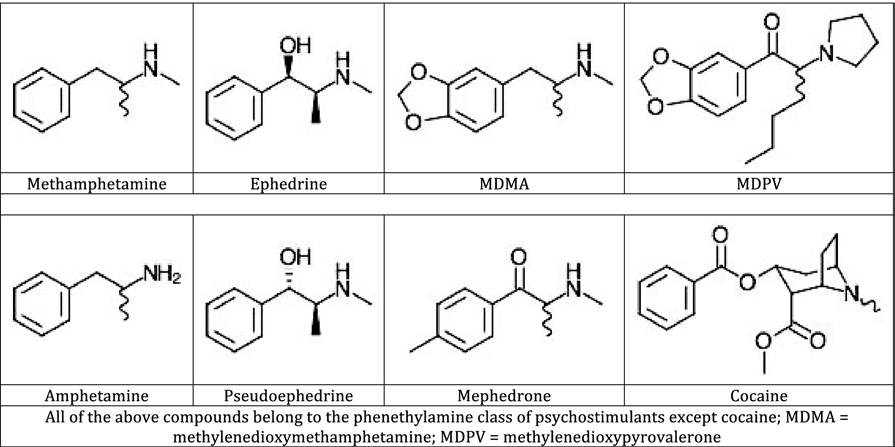 FIG 1.
FIG 1. Structures of methamphetamine and selected other psychostimulants.
Methamphetamine’s main mechanism of action is its ability to increase
neuronal release of monoamines, particularly DA
(Fig 2). Much of this
release is mediated via alterations in both the plasmalemmal dopamine
transporter (DAT) and the vesicular monoamine transporter-2 (VMAT-2).
The function of VMAT-2 in normal cells is to sequester cytoplasmic DA
into vesicles for storage and subsequent release. As such, it is an
important regulator of cytoplasmic DA
levels.13 Methamphetamine inter-
feres with the function of VMAT-2, impairing its ability to store DA into
vesicles. This effect has been shown to occur in rats as early as 1 hour
post-administration using repeated, high doses of
methamphetamine.14
This mechanism is in contrast to other sympathomimetics that act as
synaptic reuptake inhibitors, such as cocaine or methylphenidate, where
DA uptake into vesicles is
increased.15,16 Both decreased vesicular
binding and decreased vesicular uptake of DA have been demonstrated in
the presence of
methamphetamine.17,18 These actions are believed to
occur via a subcellular redistribution of vesicles containing VMAT-2. In
the presence of methamphetamine, VMAT-2 relocates from a synapto-
somal to a nonsynaptosomal location within the
neuron.19 This relocation
impairs the neuron’s ability to sequester DA within vesicles for storage
and later deposition into the synapse.
In addition to VMAT-2, cytoplasmic DA levels are also highly
regulated by DAT. Under normal conditions, DAT clears extracellular
DA from the synaptic cleft back into the nerve terminal. This reuptake of
DA is then stored into synaptic vesicles via VMAT-2 for later release.
Evidence suggests that several factors impair the normal function of DAT
46
DM, February 2012
link to page 39 link to page 39 link to page 39 link to page 38
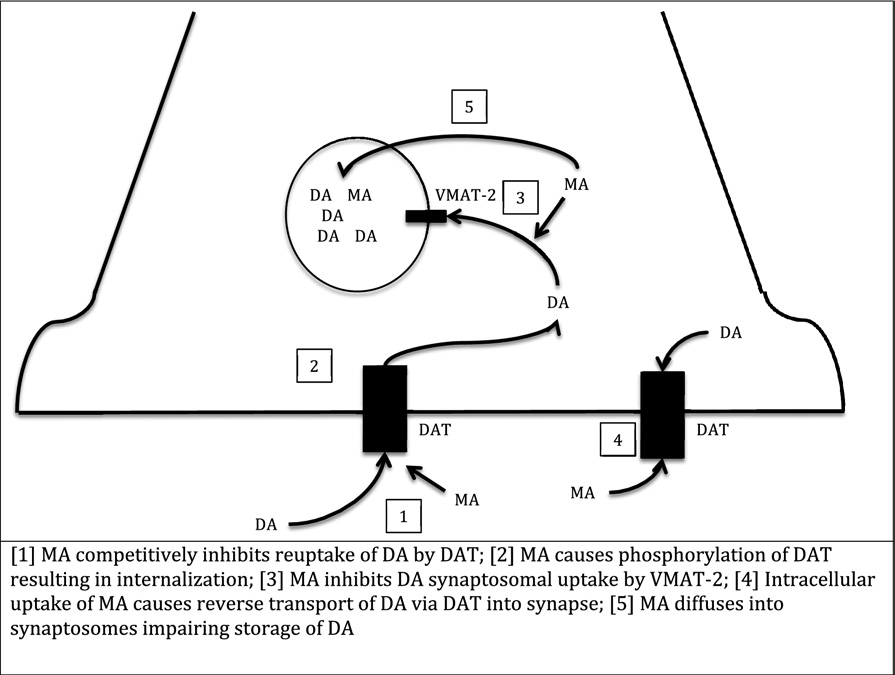 FIG 2.
FIG 2. Mechanism of action of methamphetamine on dopamine neurotransmission.
in the presence of methamphetamine. Phosphorylation of DAT via protein
kinase C occurs in response to methamphetamine, leading to internaliza-
tion of
DAT.20 Once internalized, DAT oligomers and higher molecular
weight DAT-associated protein complexes form, impairing the normal
function of
DAT.21,22 In a phosphorylation-independent mechanism,
methamphetamine also interferes with DAT reuptake of DA through
competitive
inhibition.23 Methamphetamine exists as an enantiomeric
mixture of d- and l-stereoisomers, with d-methamphetamine 3- to 10-fold
more potent at inhibiting DA reuptake via DAT than l-methamphet-
amine.13 Correspondingly, l-methamphetamine has minimal CNS effects,
whereas d-methamphetamine is the rotamer responsible for the euphoria
associated with methamphetamine abuse.
Concurrent with reuptake inhibition, methamphetamine also causes
efflux of DA into the synapse. Although the exact mechanism of this has
been debated, recent evidence suggests 2 distinct processes are involved.
Studies using amphetamine demonstrate a slow process in which amphet-
amine is transported intracellularly down its concentration gradient via
DAT in exchange for cytoplasmic DA. This transports DA out of the cell
and into the synapse in a reverse fashion through DAT compared with its
DM, February 2012
47
link to page 39 link to page 39 link to page 39 link to page 39 link to page 39 link to page 39 link to page 39
normal physiological role of DA reuptake. A second proposed mechanism
involves amphetamine inducing rapid millisecond bursts of release of
intracellular DA through DAT via a channel-like mechanism. Such a
process releases quantities of DA analogous to calcium-dependent exo-
cytosis of synaptic vesicles, and this may play a role in the psychostimu-
lant properties of
amphetamines.24 Presumably, similar mechanisms of
action occur with methamphetamine.
Synaptic DA release by methamphetamine is dependent on both
depletion of DA from vesicles and reversal of the physiological role of
DAT, with vesicular DA release being the rate-limiting
step.18,25 Impair-
ment of VMAT-2 causes relative elevations in cytoplasmic DA levels,
thus allowing transport of DA down its concentration gradient into the
synaptic cleft in the presence of methamphetamine. The chemical
properties of methamphetamine also contribute to such cytoplasmic DA
elevations. As a highly lipophilic molecule, methamphetamine freely
diffuses into nerve terminals and across vesicular membranes at high
concentrations to accumulate in synaptic vesicles. Further, as a weak
base, the accumulation of methamphetamine within these vesicles leads to
a disruption of the electrochemical gradient necessary for DA storage.
This consequently leads to elevated cytoplasmic DA concentrations and
eventual reverse transport through DAT into the
synapse.18,26
In contrast to the acute effects of increased synaptic DA efflux, repeated
high-dose administration of methamphetamine has been demonstrated to
cause persistent dopaminergic deficits in both animals and humans.
Through methamphetamine-induced aberrant cytosolic DA accumulation,
DA-associated reactive oxygen species are formed and believed to
contribute to this
depletion.18 Methamphetamine-associated reactive ox-
ygen species cause eventual activation of the Jun N-terminal kinase/
stress-activated protein kinase (JNK/SAPK) pathway, leading to neuronal
apoptosis.27 Deficits in DA nerve terminal markers (including decreases
in DA, DAT, and tyrosine hydroxylase) have been demonstrated in
postmortem studies of human
striatum.28,29 PET studies have also shown
significant loss of striatal DAT in chronic methamphetamine users.
Although abstinence has been reported to lead to some recovery in DAT,
particularly in the caudate and putamen regions, this has not been reported
to correlate with functional cognitive recovery on neuropsychological
testing.30,31 These fundamental changes underlie the neurotoxic effects
believed to cause persistent dopaminergic deficits in chronic abusers.
Chronic methamphetamine abuse has been reported to result in histo-
pathological changes in the brain. Chronic methamphetamine abuse leads
to gray- and white-matter density changes and altered concentrations of
48
DM, February 2012
link to page 40 link to page 40 link to page 40 link to page 40 link to page 40 link to page 41 link to page 41 link to page 41 link to page 41 link to page 41 link to page 41 link to page 41
metabolites in the frontal gray and white matter and anterior cingulated
gray matter that are dose-dependent and that may only be partially
reversible with
abstinence.32-36 Damage to striatal dopamine and fore-
brain serotonin terminals and degeneration of somatosensory cortical
neurons have been demonstrated in
rats.37 One of the mechanisms
thought to be responsible is methamphetamine-induced dopamine release,
resulting in reactive oxygen species, causing striatal neurotoxicity,
caspase-dependent apoptosis, and glial
activation.38-44 Advanced age and
male gender may be risk factors for more pronounced neuronal damage,
perhaps because of increased susceptibility to damage from reactive
oxygen species and the lack of protective effects of estrogen, respecti-
vely.45-47 The degree of degeneration of frontal gray- and white-matter
integrity and frontal white-matter hypometabolism has been reported to
correlate with poor performance on some neuropsychological
tests.33,47,48
Chronic methamphetamine abuse causes histopathological changes to
cardiac myocytes. Treatment of rats with methamphetamine over a period
of weeks has been reported to cause subendocardial myocytic degenera-
tion and necrosis followed by extensive myocytic degeneration, necrosis,
and
fibrosis.49 Electron microscopy of these lesions shows degeneration
of the
mitochondria.50,51 Other histopathological lesions associated with
methamphetamine abuse include myocyte hypertrophy with disorganiza-
tion of myofibrils, microtubules, and actin
structures.52 Histopathological
cardiomyocyte changes are associated with release of lactate dehydroge-
nase and creatine phosphokinase, 2 markers of cardiomyocyte damage.
Additionally, this damage may occur in the presence or absence of
beta-blockade, suggesting that methamphetamine is directly myotoxic in
addition to the toxicity that may result from sympathetic overstimula-
tion.53-55 Some of these histopathological changes may be gradually or
partially reversible following discontinuation of the
drug.56 The histo-
pathological lesions seen with chronic methamphetamine abuse are
consistent with lesions seen in cardiomyopathy and may explain the
development of cardiomyopathy in chronic methamphetamine
abusers.57
Adverse Health Effects of Methamphetamine
Abuse
Cardiovascular
Chest pain is a common complaint associated with methamphetamine
administration. Chest pain accounts for 38% of emergency department
visits and 28% of admissions in methamphetamine-intoxicated
patients.58
Tachycardia and hypertension are common clinical findings in metham-
DM, February 2012
49
link to page 41 link to page 41 link to page 41 link to page 41 link to page 42 link to page 41 link to page 42 link to page 42 link to page 41 link to page 42 link to page 42 link to page 42
phetamine
intoxication.59 Although in some patients, chest pain is due
solely to methamphetamine-induced hypertension and tachycardia or
anxiety, acute coronary syndrome (ACS) is common among methamphet-
amine users and patients with chest pain in the context of methamphet-
amine abuse should be evaluated for
ACS.60
In 1 small series of patients presenting to an emergency department with
chest pain after methamphetamine use, 25% were found to have ACS and
8% suffered a cardiac complication, including ventricular fibrillation,
ventricular tachycardia, and supraventricular
tachycardia.61 Putative
mechanisms for myocardial infarction in the setting of methamphetamine
abuse include accelerated atherosclerosis, rupture of preexisting athero-
sclerotic plaques, hypercoaguability, and epicardial coronary artery
spasm.62,63 Methamphetamine abusers have significantly higher rates of
coronary artery disease than the
public.64 Even patients with normal
coronary arteries are at risk for methamphetamine-induced myocardial
infarction because of coronary spasm, which may be refractory to
intracoronary vasodilator
therapy.63 Acute myocardial infarction follow-
ing methamphetamine use may be severe, resulting in cardiogenic shock
and
death.65
Methamphetamine is also associated with cardiac dysrhythmias. In 1
case series of methamphetamine-intoxicated patients, a prolonged
corrected QT interval (QTc ⬎440 ms) was found in 27.2% of
participants, suggesting that methamphetamine-induced alterations in
cardiac conduction may be partly responsible for its dysrhythmogenic
effects.66 Premature ventricular contractions, premature supraventric-
ular contractions, accelerated atrioventricular conduction, atrioven-
tricular block, intraventricular conduction delay, bundle branch block,
ventricular tachycardia, ventricular fibrillation, and supraventricular
tachycardia all have been reported in the setting of methamphetamine
intoxication.55,61,66 Methamphetamine-induced dysrhythmias may
also occur because of myocardial ischemia or infarction.
Methamphetamine abuse is associated with an acute dilated cardiomy-
opathy with global ventricular dysfunction. This cardiomyopathy occurs
in the absence of cardiac ischemia or infarct as measured by nuclear
myocardial perfusion study and in the absence of coronary stenosis as
measured by cardiac
catheterization.67 Methamphetamine-associated car-
diomyopathy may result in acute cardiogenic pulmonary edema and may
be
reversible.65,68,69 Several putative mechanisms by which methamphet-
amine may induce cardiomyopathy include recurrent coronary artery
spasm, small vessel disease, or diffuse myocardial toxicity because of
overstimulation of cardiac adrenergic
receptors.67 Methamphetamine-
50
DM, February 2012
link to page 42 link to page 42 link to page 42 link to page 42 link to page 42 link to page 42 link to page 42 link to page 41 link to page 42 link to page 42 link to page 42
induced cardiomyopathy has been reported to resemble transient apical
ballooning syndrome (previously known as Takotsubo cardiomyopathy),
a specific cardiomyopathy caused by transient left ventricular dysfunction
thought to be linked to excessive
catecholamines.70
Methamphetamine use may be associated with aortic dissection, likely
because of its hypertensive effects resulting in increased wall shear
stress.71 Methamphetamine appears to carry a greater risk for aortic
dissection than cocaine and may be second only to hypertension in its
importance as a risk factor for aortic
dissection.72 Aortic dissection
associated with methamphetamine abuse is also associated with cardiac
tamponade and sudden
death.73
Intravenous methamphetamine abuse has been associated with endocar-
ditis. As with other intravenous drugs of abuse, methamphetamine-
associated infective endocarditis is frequently right-sided and may result
in
death.74,75
Dermatologic
Methamphetamine abuse predisposes to repetitive, stereotypical skin-
picking, resulting in excoriations on the face and
extremities.76 In some
cases, skin picking may be related to methamphetamine-induced formi-
cation or delusions of
parasitosis.77 Both skin-picking and the use of
nonsterile needles in intravenous methamphetamine abusers may result in
skin and soft-tissue infections. In 1 series of methamphetamine abusers
presenting to an emergency department, skin infection accounted for 6%
of emergency department visits and 54% of subsequent admissions to the
hospital. Methamphetamine-related skin infections may take the form of
cellulitis or cutaneous
abscess.58
Hematological
Methamphetamine users may have a higher risk of contracting human
immunodeficiency virus (HIV) because of unsafe sex practices or use of
contaminated needles during methamphetamine administration. Metham-
phetamine users have been reported to be more likely to engage in risky
sexual behaviors than nonusers. Men who have sex with men (MSM),
heterosexual men, and heterosexual women who use methamphetamine
report more sexual partners than nonusers and more casual or anonymous
sex
partners.78 Methamphetamine users are more likely to participate in
sexual activities that confer a higher risk of HIV transmission, such as
anal sex and sex with known injection drug users, and are less likely to
use condoms during vaginal and anal
intercourse.79 Additionally, meth-
amphetamine use is associated with paying for or being paid for
sex.79
DM, February 2012
51
link to page 42 link to page 42 link to page 42 link to page 42 link to page 42 link to page 43 link to page 43 link to page 43 link to page 43 link to page 43 link to page 43
Methamphetamine use is associated with a higher risk of sexual HIV
infection.79 The use of contaminated needles is another source of HIV
infection in methamphetamine users. As with other intravenous drugs of
abuse, the sharing of needles and the corresponding risk of contracting a
blood-borne disease, including HIV, is not
uncommon.80
Methamphetamine abuse is associated with necrotizing angiitis. Histo-
logic features include fibrinoid necrosis of the intima and media of blood
vessels with destruction of vascular smooth muscle.
81,82 Macroscopically,
affected arteries display segmental narrowing with aneurysm formation,
resulting in a “beaded”
appearance.81 Drug-induced necrotizing angiitis
may result in target organ damage to the heart, brain, liver, kidney, bowel,
and pancreas with clinical manifestations of myocardial infarction,
ischemic or hemorrhagic stroke, renal failure, hepatic necrosis, bowel
infarction, and pancreatitis, among
others.83,84
Gastrointestinal
Methamphetamine users are at higher risk for contracting viral hepatitis
than nonusers because of risky sexual behavior and the use of contami-
nated needles. Methamphetamine users are more likely to be infected with
hepatitis A and B than nonusers and, among methamphetamine users,
injection users have a higher prevalence of both diseases than noninjec-
tion
users.85 Use of contaminated needles puts methamphetamine users at
particular risk for hepatitis C infection, although hepatitis C infection is
also more common among methamphetamine users who smoke or
insufflate the drug than it is in the general
population.86,87
Even in the absence of viral hepatitis, methamphetamine abuse has been
reported to cause acute liver injury with hepatic necrosis and centrilobular
degeneration.88 Additionally, methamphetamine enhances the hepatic
toxicity of other agents, such as carbon tetrachloride. Although the cause
of the hepatic injury is unclear, it has been proposed that an adrenore-
ceptor-related mechanism or stimulation of Kupffer cells may be respon-
sible.89,90
Mesenteric infarction requiring total proctocolectomy and resection of
the ileum and jejunum has been reported following methamphetamine use
with microscopic examination showing changes consistent with acute
vasculitis.91 Segmental ischemic colitis in the absence of thrombosis,
vasculitis, or vasospasm with spontaneous resolution has also been
reported.92 Methamphetamine may cause mesenteric ischemia or infarc-
tion by several mechanisms, including necrotizing vasculitis, cardiovas-
cular shock, sympathomimetic vasospasm, or splanchnic vasoconstric-
52
DM, February 2012
link to page 43 link to page 43 link to page 42 link to page 43 link to page 43 link to page 43 link to page 43 link to page 17 link to page 43 link to page 44 link to page 44 link to page 44
tion.93-95 It remains unclear how important each of these mechanisms is
to methamphetamine-induced mesenteric infarction.
Severe acute necrotic hemorrhagic pancreatitis has been reported in
cases of sudden death in chronic methamphetamine abusers. Histopathol-
ogy studies of the effect of chronic methamphetamine abuse on pancreatic
tissues suggest that methamphetamine may cause regional hemorrhage,
acinal cell death, and fibrosis possibly because of tissue hypoxia or
necrotizing
angiitis.96,97
Genitourinary
Methamphetamine users are more likely to be diagnosed with a sexually
transmitted disease (STD) than nonusers because of an increased likeli-
hood of engaging in risky sexual
behaviors.78,79 Prolonged sex while on
methamphetamine can lead to chafing or soft-tissue injury to the genitals
with correspondingly higher risk of transmission of an STD or blood-
borne infection.
98 Injection methamphetamine abusers have a higher
prevalence of STD infections than noninjection methamphetamine abus-
ers.99 Among methamphetamine-dependent gay men, an elevated preva-
lence of chlamydia, syphilis, and genital and oral gonorrhea has been
reported with a lifetime prevalence of genital gonorrhea of 40%. Psychi-
atric comorbidity may be associated with a higher prevalence of STD
infection in methamphetamine-dependent individuals.
100 In 1 study in
Thailand, methamphetamine users were reported to have higher rates of
chlamydial infection than opiate
users.101
Musculoskeletal
Perhaps the most publicized adverse health effect of methamphetamine
abuse, by both governmental agencies and the lay media, is “meth mouth”
(Fig 3).102,103 Methamphetamine induces dental decay through multiple
mechanisms, including xerostomia from sympathetic overstimulation and
bruxism, resulting in multiple dental
caries.104,105 Also of concern is the
consumption of large quantities of sugared soft drinks in an attempt by the
user to resolve the xerostomia and lack of oral hygiene during extended
periods of drug
abuse.106,107 Although dental decay because of metham-
phetamine abuse is well documented, 1 study found that the degree of
dental decay in methamphetamine users as compared to other substance
users in an inpatient chemical dependency treatment unit was similar,
suggesting that at least some of the dental decay associated with
methamphetamine abuse is due to factors common to substance abuse in
general, such as poor personal hygiene and
malnutrition.108
DM, February 2012
53
link to page 44 link to page 41 link to page 44 link to page 44
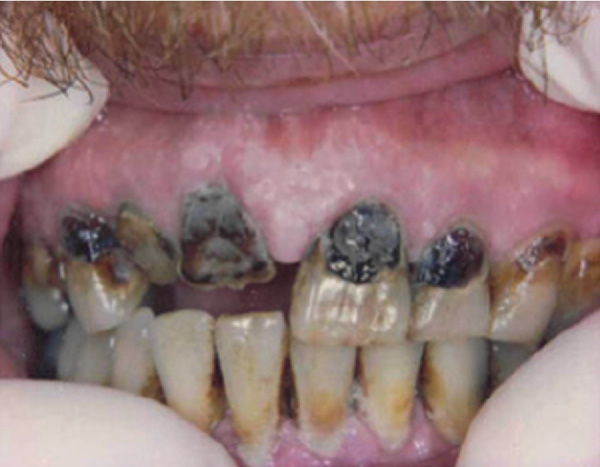 FIG 3.
FIG 3. “Meth mouth.” Severe dental caries because of methamphetamine abuse. (Reprinted
with permission from Hamamoto DT, Rhodus NL. Methamphetamine abuse and dentistry. Oral
Dis 2009;15:27-37.) (Color version of figure is available online.)
Methamphetamine abuse is also associated with rhabdomyolysis. In 1
series of patients presenting to an emergency department with rhabdo-
myolysis, 43% had urine drug immunoassays positive for methamphet-
amine. Methamphetamine-induced rhabdomyolysis may be due to psy-
chomotor agitation or
seizures.109
Methamphetamine-intoxicated patients are at increased risk for trau-
matic injury. In 1 case series of methamphetamine-positive patients
presenting to an emergency department, the most common chief com-
plaint was blunt trauma, accounting for 33% of emergency department
visits and 74% of subsequent
admissions.58 Among a case series of
consecutive trauma patients, methamphetamine was the most commonly
used illicit drug. Trauma patients with positive urine drug immunoassays
for methamphetamine are more likely to suffer from violent mechanisms
of injury, including assault, gunshot wound, and stabbing than trauma
patients testing negative for methamphetamine. They are also more likely
to have attempted suicide, be a victim of domestic violence, or have an
altercation with law
enforcement.110,111 Methamphetamine users have
also been reported to be more likely to have severe injuries, to leave
against medical advice, and to die from their
injuries.110,112
Pott’s puffy tumor (osteomyelitis of the frontal bone) has been associ-
ated with intranasal methamphetamine use. Local methamphetamine-
induced ischemic injury to the sinus mucosa is thought to produce an
54
DM, February 2012
link to page 44 link to page 44 link to page 44 link to page 42 link to page 42 link to page 44 link to page 42 link to page 44 link to page 44 link to page 44 link to page 43 link to page 44 link to page 41 link to page 45
environment conducive to the development of frontal bone osteomyelitis
and subperiosteal
abscess.113
Neurological
Methamphetamine is associated with many neurological adverse health
effects, although the most devastating is intracranial hemorrhage. Meth-
amphetamine-induced hypertension and tachycardia may lead to intracra-
nial hemorrhage, in patients with or without preexisting cerebrovascular
disease.114 Methamphetamine may be more toxic than cocaine in induc-
ing intracranial hemorrhage, possibly because of its more prolonged
cardiovascular
effects.115 Methamphetamine-induced necrotizing angiitis
may also play a role in methamphetamine-associated intracranial hemor-
rhage with fibrinoid necrosis of the intima and media of vessels
predisposing to vessel
rupture.81,116,117 Intraparenchymal bleeds in the
cerebrum, cerebellum, corpus callosum, basal ganglia, and brainstem
have been reported and may result in
death.81,114,116-119 Fatal intraven-
tricular hemorrhages have also been
reported.120 A number of intracranial
berry aneurysm ruptures related to methamphetamine intoxication have
been reported, frequently with fatal
results.73,115 Subarachnoid hemor-
rhage in the absence of berry aneurysm or arteriovenous malformation
has also been
reported.117
Methamphetamine abuse is also associated with ischemic
stroke.119,121-123
As with intracranial hemorrhage, methamphetamine-induced hyper-
tension, tachycardia, and necrotizing angiitis may contribute to the
development of ischemic
stroke.121 For intravenous methamphetamine
use, fillers, such as talc, may also contribute to ischemic or hemorrhagic
stroke.94 Methamphetamine-induced ischemic stroke may occur in the
absence of evidence of chronic hypertension or cerebral vasculopa-
thy.117,119
Methamphetamine intoxication also causes seizure. Methamphetamine-
induced seizures may occur in persons with or without any past medical
history of seizure disorder. In 1 series of methamphetamine-intoxicated
patients presenting to an emergency department, 7% of patients with
altered level of consciousness had tonic-clonic seizure and, of those
patients, 75% had no previous history of
seizure.58 Limited evidence
suggests that chronic methamphetamine exposure may lower the seizure
threshold more than a single acute
exposure.124
Methamphetamine abuse also results in cognitive impairment, which
may be persistent. Current methamphetamine users have impaired per-
formance on tests of memory, the ability to manipulate information,
attention, and abstract thinking as compared to matched controls, al-
DM, February 2012
55
link to page 45 link to page 45 link to page 38 link to page 45 link to page 45 link to page 45 link to page 45 link to page 45 link to page 45 link to page 45 link to page 45 link to page 45 link to page 45
though they showed no impairment in psychomotor speed, intelligence, or
verbal fluency. Heavier methamphetamine users have greater cognitive
impairment than less frequent
users.125 Methamphetamine may selec-
tively impair visual memory more than verbal memory, perhaps
because of executive function
damage.126 Conversely, at low admin-
istered doses, some studies have reported that single doses of
methamphetamine may improve reaction times, cognitive perfor-
mance, and verbal
memory.10,127
Following methamphetamine abstinence of 1-2 weeks, chronic
methamphetamine abusers show persistent impairment on neurocog-
nitive measures of attention, psychomotor speed, verbal learning and
memory, and executive system
measures.128 Following prolonged
methamphetamine abstinence (mean abstinence of 20 months),
chronic methamphetamine abusers still display impaired attentional
control that may be related to changes in neurochemicals in frontos-
triatal brain regions and to microstructural changes in the white matter
of the corpus
callosum.129,130
Patients with HIV or hepatitis C may be particularly at risk for
developing cognitive impairment because of methamphetamine abuse.
Hepatitis C infection augments methamphetamine-induced cognitive
deficits in the areas of learning, abstraction, and motor skills as well
as global neuropsychological
impairment.131 HIV similarly interacts
with methamphetamine to produce cognitive
deficits.132 HIV-positive
chronic methamphetamine users display additional neuronal injury
and glial activation in the frontal cortex and basal ganglia as compared
to HIV-negative methamphetamine
users.133 This effect is amplified in
patients with high HIV viral
loads.134 A combination of methamphet-
amine and HIV proteins has been implicated in causing significant
neuronal toxicity, possibly by activating caspase-dependent cell death
pathways leading to neuronal
apoptosis.135-137
Rarely, methamphetamine abuse has been associated with choreoathe-
tosis. This may be due to central dopaminergic effects of methamphet-
amine and has been reported only in the setting of acute methamphet-
amine
intoxication.138,139 Other reported neurological sequelae of
methamphetamine intoxication include photophobia and
ataxia.140
Ophthalmologic
Acute unilateral vision loss has been reported following intranasal
methamphetamine abuse. The vision loss is believed to be due to ischemic
optic neuropathy secondary to methamphetamine-induced vasospasm and
methamphetamine-associated
vasculitis.141,142
56
DM, February 2012
link to page 46 link to page 46 link to page 42 link to page 46 link to page 46 link to page 41 link to page 43 link to page 46 link to page 46 link to page 46 link to page 46 link to page 46 link to page 46 link to page 46 link to page 46
Psychiatric
Methamphetamine abuse is associated with psychiatric disease. Meth-
amphetamine intoxication is associated with restlessness, insomnia,
hallucinations, paranoia, and disturbance of
consciousness.143 Abstinence
following methamphetamine intoxication is associated with depression,
anhedonia, irritability, and poor concentration, although these symptoms
are frequently mild and transient.
144 Methamphetamine users are more
likely to carry a psychiatric diagnosis and be prescribed psychiatric
medications than cocaine
users.80
Chronic methamphetamine abuse is associated with depressive symp-
toms and suicidal ideation.
145,146 Among adolescent methamphetamine
users, 16% reported suicidal
ideation.147 Suicide attempts during meth-
amphetamine intoxication are common and may involve overdose, slash
wounds to the extremities, and jumps from
heights.58,148 In methamphet-
amine-dependent gay men, 25% report a history of at least 1 suicide
attempt.
100 In 1 series of completed youth suicides, alcohol and metham-
phetamine were the most common substances found in the
blood.149 Risk
factors for methamphetamine-related suicide attempt include female
gender, intravenous methamphetamine use, history of methamphetamine-
induced psychosis, methamphetamine-induced depressive disorder, and
family history of psychotic disorders.
150,151
Methamphetamine abuse may be associated with self-injurious behavior
and self-mutilation. Methamphetamine-intoxicated individuals may be
motivated by bizarre religious, sexual, or neurotic thoughts and self-
mutilation may take a variety of forms, such as eye enucleation or genital
self-mutilation.152 In some chronic methamphetamine abusers, self-
mutilation may be recurrent or
severe.153
Chronic methamphetamine abuse may result in psychosis with predom-
inant auditory hallucinations, persecutory delusions, delusions of refer-
ence, and pathologic hostility.
154-157 Methamphetamine-induced psycho-
sis mimics paranoid schizophrenia and patients with either disease have
been found to have similar deficits in neurocognitive
functioning.158 In 1
sample of methamphetamine abusers, 13% screened positive for psycho-
sis, whereas another 23% had at least 1 psychotic symptom (eg,
unusual thought content). Dependent methamphetamine abusers were
3 times more likely to have psychotic symptoms than nondependent
abusers, and the prevalence of psychosis in methamphetamine abusers
was reported to be 11 times higher than in the general
population.159
In Thailand, 10% of psychiatric hospital admissions are for metham-
phetamine-related
psychosis.160
DM, February 2012
57
link to page 46 link to page 47 link to page 46 link to page 47 link to page 42 link to page 47 link to page 47 link to page 47 link to page 47 link to page 47 link to page 43
Chronic methamphetamine abuse results in behavioral sensitization to
the drug where even small doses may then trigger a relapse of the
psychosis and the duration of vulnerability to relapse progressively
becomes
longer.161,162 Although in some patients methamphetamine
psychosis may be transient, in others psychosis may persist despite
months of abstinence and be resistant to antipsychotic
medications.163
Young age at onset of methamphetamine abuse, heaviness of metham-
phetamine abuse, schizoid or schizotypal personality disorder, and history
of preexisting neurological disorder (eg, learning disorder or attention-
deficit/hyperactivity disorder) are risk factors for the development of
persistent methamphetamine-induced
psychosis.155,164 In addition, the
extent of neuronal damage in the basal ganglia correlates with severity of
psychiatric
symptoms.165
Pulmonary
Acute noncardiogenic pulmonary edema may occur after smoking
methamphetamine despite normal pulmonary artery and pulmonary
wedge pressures. Respiratory failure and hypotension requiring mechan-
ical ventilation and vasopressor support have been reported and have been
reported to be
reversible.68
Methamphetamine is strongly associated with idiopathic pulmonary
arterial hypertension
(PAH).166 Methamphetamine intoxication has been
shown to cause an acute rise in pulmonary arterial
pressures.167 Although
the role methamphetamine plays in inducing PAH remains unclear,
proposed mechanisms include toxic endothelial injury, hypoxic insult,
direct spasm, vasculitis, and dysregulation of vascular
tone.168 One
favored hypothesis is that methamphetamine induces PAH by the same
mechanism as fenfluramine, through interaction with serotonin transport-
ers resulting in serotonin
release.169
An additional concern in methamphetamine-induced PAH is the use of
outpatient intravenous therapy. In severe cases of PAH, continuous
epoprostenol or treprostinil infusions may be indicated and infused in the
outpatient setting through an indwelling central intravenous catheter. Use
of such indwelling catheters in methamphetamine users may be compli-
cated by homelessness, inability to properly care for the catheter, or
infection because of the patient accessing the catheter to administer illicit
drugs.170
Renal
Acute renal failure may be reported following methamphetamine abuse
and may be due to myoglobinuria, hypotension, or necrotizing
angiitis.91
58
DM, February 2012
link to page 44 link to page 43 link to page 47 link to page 47 link to page 47 link to page 47 link to page 47 link to page 47 link to page 47 link to page 48 link to page 48 link to page 48 link to page 48 link to page 48
Myoglobinuric renal failure because of methamphetamine-associated
rhabdomyolysis is frequently self-limited, although hemodialysis may be
temporarily necessary. Rarely, methamphetamine-associated myoglobin-
uric renal failure may be persistent, resulting in end-stage renal dis-
ease.109 Methamphetamine-associated necrotizing angiitis has also been
associated with renal insufficiency culminating in end-stage renal disease
requiring
hemodialysis.84
Obstetrical
Methamphetamine is increasingly a drug of choice among substance-
dependent pregnant
women.171 Methamphetamine abuse during preg-
nancy is concerning both for the risk of adverse pregnancy outcome and
for possible damage to the developing fetus. Methamphetamine abuse is
also associated with perinatal maternal death and has been implicated as
a possible contributing factor to amniotic fluid embolism.
Several adverse pregnancy outcomes have been associated with prenatal
maternal methamphetamine use. Methamphetamine use is associated with
fetal growth restriction and premature
delivery.172-175 Placental insuffi-
ciency, hemorrhage, and abruption have also been associated with
maternal methamphetamine
abuse.175,176 Prenatal methamphetamine ex-
posure is thought to put a fetus at higher risk for intraventricular
hemorrhage and cavitary lesions in the
brain.175 Additionally, maternal
methamphetamine abuse is associated with inadequate prenatal
care.177
Prenatal exposure to methamphetamine has been suggested to increase
the risk for adverse postnatal outcomes. Prenatal methamphetamine
exposure has been linked to neonatal neurobehavioral outcomes of
decreased arousal, increased physiological stress, and poor quality of
movement in a dose–response
relationship.178,179 Prenatal methamphet-
amine exposure has been reported to cause neonatal toxic hepatitis with
cholestasis.180 Children with prenatal methamphetamine exposure have
been noted to have structural and chemical brain differences as compared
to healthy controls and structural differences correlate with poorer
performance on attention and verbal memory
tests.181,182 Animal studies
have also suggested that prenatal methamphetamine exposure may
adversely affect the myelination
process.183 Rats exposed prenatally to
methamphetamine are reported to have lower seizure threshold, lower
birth weights, and impaired sensory-motor
coordination.184,185 Rat stud-
ies have also suggested that some methamphetamine-related deficits, such
as sensory-motor correlation, may affect 2 generations of
offspring.186
Although methamphetamine has been reported to be teratogenic in animal
studies, no human studies have confirmed this
effect.187,188
DM, February 2012
59
link to page 48 link to page 48 link to page 48 link to page 48 link to page 48 link to page 48 link to page 48 link to page 48
Exploratory Methamphetamine Exposure in Children
Inadvertent pediatric exposure to methamphetamine may be increasing.
In 1 series of methamphetamine-dependent patients presenting for drug
rehabilitation, 44% had children in their home. Of children found in
methamphetamine laboratories by police or child protective services, 45%
have a positive hair specimen for 1 or more illicit drugs with the most
common positive result being
methamphetamine.189 Common signs and
symptoms of methamphetamine poisoning in the pediatric population
include tachycardia, agitation, inconsolable crying, irritability, and vom-
iting. Rhabdomyolysis is a common complication.
190,191 Seizure is a less
common symptom of pediatric methamphetamine
poisoning.191 Transient
cortical blindness secondary to methamphetamine poisoning has been
reported in an
infant.192 Pediatric methamphetamine poisoning may be
difficult to distinguish from scorpion envenomation, resulting in unnec-
essary exposure to
antivenom.190,193
Children may also be at risk of traumatic injury or abuse because of
parental behaviors while using methamphetamine. Parental supervision
while on a methamphetamine binge may be lax and caregivers may sedate
their children with benzodiazepines or diphenhydramine while engaging
in methamphetamine abuse. In addition, children in homes where meth-
amphetamine is abused are reported to be at higher risk for exposure to
age-inappropriate material, such as pornography.
189
Methamphetamine-Associated Death
Methamphetamine abuse may be directly or indirectly fatal. Direct
methamphetamine-related mortality is frequently due to catastrophic
neurological or cardiac complications, while indirect methamphetamine-
related deaths are frequently traumatic in nature. In 1 series of metham-
phetamine-related fatalities, the cause of death was categorized as natural,
accidental, suicidal, homicidal, or uncertain in 13%, 59%, 11%, 14%, and
3% of cases, respectively. In another series, homicide and suicide
accounted for 27% and 15% of methamphetamine-related fatalities,
respectively.194 In a series of autopsies in methamphetamine-positive
patients, the most common cause of death was multiorgan system
dysfunction, followed by cardiovascular or cerebrovascular disease,
traumatic shock, asphyxiation, and
exsanguination.195
Methamphetamine-related fatalities constitute a significant public
health problem in areas where methamphetamine abuse is prominent: in
Taiwan, 12.1% of all autopsy cases in 1 year were related to metham-
60
DM, February 2012
link to page 48 link to page 48 link to page 48 link to page 48 link to page 49 link to page 49 link to page 44 link to page 49 link to page 42 link to page 42 link to page 49 link to page 48 link to page 49
phetamine. Males may be more likely to suffer methamphetamine-related
death than
females.195,196
Concomitant abuse of another drug, eg, cocaine or ethanol, has been
identified as a factor in some methamphetamine-related fatalities and
varies in frequency depending on cultural
norms.197 Although animal
studies have suggested that concomitant ethanol ingestion is protective
against some of the toxic effects of methamphetamine, ethanol intoxica-
tion may simultaneously increase the risk of accidental or traumatic
death.198
A frequently reported cause of direct methamphetamine-related fatality
is multisystem organ failure secondary to methamphetamine toxicity,
which is characterized by hyperthermia, pulmonary congestion, coma,
shock, hyperthermia, acute renal failure, metabolic acidosis, and hyper-
kalemia.195,198-200 As with other illicit drugs, body packers and body
stuffers are at risk for death in the event of package
rupture.201-203
Methamphetamine-induced agitation and hyperactivity can cause death
secondary to metabolic acidosis and
hyperthermia.204
Intracranial hemorrhage is a commonly reported neurological compli-
cation of methamphetamine abuse resulting in
death.118 Methamphet-
amine-related status epilepticus may also contribute to
death.202 Cardiac
complications of methamphetamine abuse that are frequently reported to
result in death include arrhythmia and acute myocardial
infarction.65,66
Methamphetamine-related hypertension and tachycardia may cause sud-
den death because of berry aneurysm rupture or aortic dissection with
cardiac
tamponade.73
Indirect methamphetamine-related fatalities are frequently traumatic
and may be due to accident, assault, or
suicide.205 Methamphetamine-
related traffic deaths could result from riskier driving behavior while
intoxicated, and blood amphetamine concentration is positively correlated
to traffic-related
impairment.194,206,207 In 1 study of traffic-related fatal-
ities, methamphetamine was found in the blood of 5% of fatally injured
drivers.208
Methamphetamine Abuse-Associated Toxicologic
Exposures
Most reported toxicologic exposures because of methamphetamine are
in the context of production of methamphetamine, discussed below.
However, methamphetamine abuse has been linked to acute lead poison-
ing. Depending on the method of synthesis used, methamphetamine
manufacture may involve lead acetate. Lead poisoning due to metham-
phetamine abuse may be due to a high lead content in the drug because
DM, February 2012
61
link to page 49 link to page 49 link to page 49 link to page 38 link to page 38 link to page 49 link to page 49
of inadequate processing during manufacture or deliberate contamina-
tion.209 In 1 outbreak of methamphetamine-associated lead poisoning, 14
confirmed cases occurred in 1 year because of intravenous use of a batch
of methamphetamine that was 60% lead by
weight.210 However, lead
poisoning is not thought to be widespread among methamphetamine users
and may occur only episodically with batches of contaminated
drug.211
Current Trends
Domestic Trends
Several agencies collect data useful in identifying trends in metham-
phetamine use. A frequent limitation in these data sets is the inclusion of
methamphetamine in a general category labeled “non-cocaine stimu-
lants,” making it difficult to track trends in methamphetamine as opposed
to trends in stimulant abuse in general. Examples of national data sources
include the National Survey on Drug Use and Health, Monitoring the
Future, Youth Behavior Risk Surveillance System, Treatment Episode
Data Set, Drug Abuse Warning Network, Substance Abuse and Mental
Health Services Administration, and Arrestee Drug Abuse Monitoring
system.1
A 2004 report issued by Substance Abuse and Mental Health Services
Administration estimates that, in 2004, 12 million or 2.9% of the US
population aged 12 years or older have tried methamphetamine in their
lifetime; 1.4 million used it in the past year, and 600,000 used it in the
past month. The highest rates of past year methamphetamine use were
found among Native Hawaiians or Pacific Islanders (2.2%) and American
Indians or Alaska Natives (1.7%), whereas lower rates of past year use
were found among whites (0.7%), Hispanics (0.5%), blacks (0.1%), and
Asians
(0.2%).1 Another survey estimates rates of past year methamphet-
amine use among persons aged 12 or older were highest in Nevada
(2.0%), Montana (1.5%), and Wyoming (1.5%), while the lowest rates
were in Connecticut, Maryland, Massachusetts, New Jersey, and New
York.212-214 The highest rates of amphetamine- or methamphetamine-
related emergency department visits are reported in San Francisco,
Seattle, San Diego, and Los Angeles. In the 2002 Drug Abuse Warning
Network database, white patients were responsible for 65% of amphet-
amine- or methamphetamine-related emergency department visits; 58%
of visits were men, and most visits involved patients aged 18-34
years.215,216
Subpopulations at disproportionate risk for methamphetamine use
reportedly include criminal offenders and MSM. Currently, men and
62
DM, February 2012
link to page 38 link to page 49 link to page 27 link to page 49 link to page 50 link to page 50
women abuse methamphetamine equally, unlike many other illegal drugs
where there is a male predominance among abusers. Methamphetamine
abusers frequently engage in criminal and/or violent behavior and many
have been involved with the criminal justice system.
Among MSM, methamphetamine abuse is associated with high-risk
sexual behaviors. Methamphetamine is increasingly abused by MSM
while engaging in sexual activity, termed “party and play” or “PnP,” and
abuse is common in sex clubs and “circuit
parties.”1,8,217 The number of
methamphetamine laboratories seized by USA law enforcement agencies
increased by 25% between 2001 and
2004.214 Methamphetamine labora-
tory incidents, defined as discovery of laboratories, dumpsites, or meth-
amphetamine manufacture equipment, also continue to increase. In March
2009, 966 methamphetamine laboratory incidents were reported nation-
ally, an increase from 756 in March 2008 and 596 in March 2007. A total
of 11,239 methamphetamine laboratory incidents were reported nation-
ally in calendar year 2010, with the majority of incidents and the largest
increases occurring in the Midwest and the South
(Fig 4).218,219
Global Trends
International trends show increasing amphetamine use. The 2011
United Nations Office of Drugs and Crime estimates annual prevalence of
amphetamine-type stimulants as the second most widely used illicit drug
in the world, following cannabis. Amphetamines, which include meth-
amphetamine, amphetamine, and methcathinone, are used by 14-56
million people worldwide in 2009, with more specific estimates made
difficult by uncertainty in abuse rates in China and India. Of the
amphetamine-type stimulants, methamphetamine is estimated to be the
most widely manufactured. Asia manufactures a substantial proportion of
the worldwide production of methamphetamine, with methamphetamine
manufacture being particularly prevalent in East and Southeast Asia,
including the Philippines, China, Myanmar, and Malaysia. Global sei-
zures of amphetamine-type stimulants have more than tripled between
1998 and 2009, a much faster rate of increase than has been seen with
seizures of cocaine, heroin, morphine, and cannabis. Methamphetamine
seizures were most common in Oceania, Africa, North America, and
Asia. It is estimated that the majority of methamphetamine laboratories
dismantled worldwide are located in North
America.220
Clandestine Methamphetamine Laboratories
Clandestine methamphetamine laboratories are operated throughout the
USA and make up over 80% of clandestine drug
laboratories.221 In 2008,
DM, February 2012
63
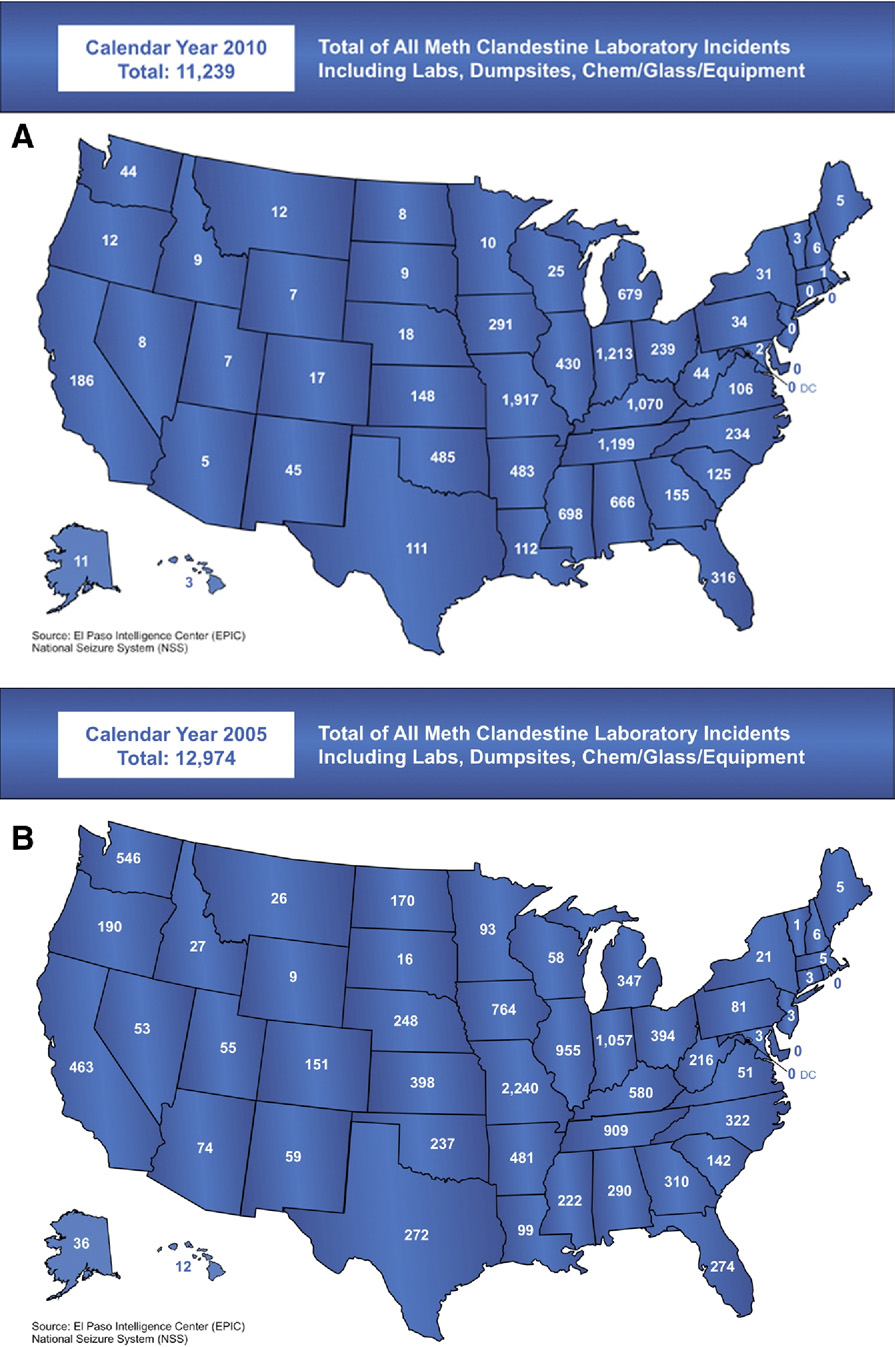 FIG 4.
FIG 4. Trends in meth clandestine laboratory incidents in the USA in (A) 2010 and (B) 2005.
(Source:
http://www.justice.gov/dea/concern/map_lab_seizures.html.) (Color version of fig-
ure is available online.)
64
DM, February 2012
link to page 41 link to page 28 link to page 50 link to page 50 link to page 50 link to page 50 link to page 50 link to page 50 link to page 50 link to page 50
 FIG 5.
FIG 5. Illicit meth lab in a bedroom. (Reprinted with permission from Methamphetamine
Awareness and Prevention Project of South Dakota
[http://www.mappsd.org/].) (Color
version of figure is available online.)
6783 methamphetamine laboratories were found, predominantly in the
Midwest.61 Laboratories vary in size from “mom-and-pop” operations to
large-scale “super labs”
(Fig 5).222
Illicit drug manufacturers, also known as “cooks,” may obtain their
“recipes” from other cooks, the chemistry literature, underground culture/
resources, or the
Internet.222 Methamphetamine can be made using
several different techniques, none of which are safe outside the clinical
laboratory. The first method used in the manufacture of illicit metham-
phetamine was developed in the 1960s and involved the precursor
chemical phenyl-2-propanone (P2P). P2P was combined with alcohol and
an aluminum amalgam, usually aluminum foil or wire mixed with a small
amount of mercuric chloride, and allowed to react
overnight.223 The
methamphetamine is then isolated using hydrochloric acid, organic
solvents, and
filters.222
A second method using the precursor chemical P2P combined it with
N-methylformamide and formic acid in the Leuckart reaction; the
intermediate is then refluxed with hydrochloric acid to form methamphet-
amine.222-224 In 1980, the Drug Enforcement Administration made P2P
a Schedule II controlled substance, which led to the illicit manufacture
of
P2P.225 Phenylacetic acid can be combined with acetic anhydride,
lead acetate, or acetic acid with pyridine to form
P2P.222-224 Other
methods of manufacturing P2P involve thorium oxide and pumice or
benzyaldehyde and
nitroethane.222,223 The Chemical Diversion and
DM, February 2012
65
link to page 50 link to page 50 link to page 50 link to page 50 link to page 50 link to page 50 link to page 50 link to page 50 link to page 50 link to page 50 link to page 50 link to page 50 link to page 30 link to page 31
Trafficking Act of 1987 placed restrictions on P2P precursors, forcing
illicit methamphetamine producers to manufacture their own pheny-
lacetic acid. This can be accomplished using benzyl cyanide or
benzylchloride.222
The Drug Enforcement Administration classification of P2P as a
Schedule II controlled substance also led methamphetamine manufac-
turers to seek out new methods by which to produce the
drug.225 In the
early 1980s, methamphetamine manufacturers found that reacting
ephedrine and pyridine with hydrogen iodide and red phosphorus in
carbon disulfide was effective in producing
methamphetamine.223
Ephedrine and pseudoephedrine remain the most popular precursor
chemicals today, because of ease of procurement in common over-
the-counter cold
medicines.222 E sinica can also be used as a source
for ephedrine and
pseudoephedrine.226
Currently, there are 2 methamphetamine-manufacture methods using
ephedrine or pseudoephedrine as a precursor chemical, both with the
common goal of removing a hydroxyl group from the precursor: the
cold or red phosphorus method and the Nazi or Birch method. The
ephedrine or pseudoephedrine is extracted from over-the-counter
medications using water or alcohol and
heat.222 The cold method uses
red phosphorous and hydriodic acid to convert ephedrine/pseu-
doephedrine to
methamphetamine.227 Historically, Freon was used to
extract the finished product, but other organic solvents may be used as
well.222 Hydriodic acid frequently must be illicitly manufactured
because of restrictions placed on it as
well.222 In the Nazi/Birch
method, an alkali metal (typically sodium or lithium) is combined with
anhydrous ammonia and the ephedrine or pseudoephedrine and then
subsequently with water or alcohol and hydrogen chloride gas to form
methamphetamine.222-224 This method is called the Nazi method
because of the widespread belief that it was invented by the Nazis
during World War
II.228
The most recently reported method for making methamphetamine is
called “shake and bake.” The “shake and bake” method requires less
pseudoephedrine, a 2-L soda bottle, and no heat source. The pseu-
doephedrine is crushed and ammonium nitrate is added. This method
can be done anywhere, including in a moving vehicle. A small amount
of methamphetamine is produced using this method, making it useful
for individuals attempting to manufacture their own methamphetamine
but not for larger scale
laboratories.229,230 Tables 3 and
4 list common
chemicals and equipment used in the manufacture of methamphet-
amine.
66
DM, February 2012
link to page 50
TABLE 3. Chemicals used in illicit methamphetamine
manufacture222,228,230
Chemical
Where It Is Used
Common Sources
Acetic acid
P2P synthesis
Vinegar
Acetic anhydride
P2P synthesis
Acetone
Solvent
Paint thinner, nail polish
remover
Acetylene gas
Gas purge
Welding gas
Aluminum
P2P synthesis
Aluminum foil/wires
Anhydrous ammonia
Methamphetamine synthesis
Farm fertilizer
Ammonium nitrate
Methamphetamine synthesis
Fertilizer, cold compress packs
Benzaldehyde
P2P synthesis
Benzene
Solvent
Benzylchloride
Phenylacetic acid synthesis
Benzyl cyanide
Phenylacetic acid synthesis
Ephedrine
Methamphetamine precursor
Cold preparations
Ethanol
Solvent
Alcohol
Ethyl ether
Solvent
Engine starting fluid
Formic acid
Solvent
Freon
Solvent
Refrigeration systems
Hydriodic acid
Methamphetamine synthesis
Hydrochloric acid/gas
Solvent (acid),
Swimming pool supplies
(muriatic acid)
methamphetamine
synthesis (gas)
Hydrogen gas
Gas purge,
methamphetamine
synthesis byproduct
(lithium reacting with
water)
Hydrogen sulfide
Hydriodic acid synthesis
Hypophosphorous acid
Methamphetamine synthesis
Iodine
Hydriodic acid synthesis
Farming and health care
supplies
Isopropanol
Solvent
Rubbing alcohol
Lead acetate
P2P synthesis
Lithium
Methamphetamine synthesis
Photo batteries
Magnesium sulfate
Methamphetamine synthesis
Epsom salts
Mercuric chloride
Methamphetamine synthesis
Methanol
Solvent
Heet®, gasoline additives
Methylamine
Methamphetamine precursor
N-methylformamide
Methamphetamine precursor
Nitroethane
P2P precursor
Petroleum distillates
Solvent
Coleman fuel, kerosene, lacquer
thinner, mineral spirits,
naphtha, lighter fluid
Phenyl-2-propanone (P2P)
Methamphetamine precursor
Phenylacetic acid
P2P precursor
Phosphine gas
Methamphetamine synthesis
byproduct
Phosphoric acid
Methamphetamine precursor
Rust remover, colas
Pseudoephedrine
Methamphetamine precursor
Cold preparations
Pyridine
P2P synthesis
DM, February 2012
67
link to page 50 link to page 50 link to page 50 link to page 50 link to page 50 link to page 50 link to page 51
TABLE 3. Continued
Chemical
Where It Is Used
Common Sources
Red phosphorous
Methamphetamine synthesis
Road flares, matchbook strikers
Sodium
Methamphetamine synthesis
Sodium acetate
P2P synthesis
Sodium chloride
Methamphetamine synthesis
Table salt
Sodium hydroxide
Methamphetamine synthesis
Red devil lye
and byproduct
Sulfuric acid
Methamphetamine and P2P
Battery acid, drain cleaners
synthesis
Thorium oxide
P2P synthesis
Toluene
Synthesis/solvent
Brake cleaner
Trichloroethane
Methamphetamine synthesis
Gun scrubber/cleaner
TABLE 4. Equipment frequently used in illicit methamphetamine
manufacture253,258
Aluminum foil
Blenders
Cheesecloth
Clamps
Coffee filters
Funnels
Gas cans
Hot plates
Ice chests
Jugs and bottles
Kitty litter
Laboratory beakers/glasses
Measuring cups
Pails/buckets
Paper towels
Plastic storage containers
Propane cylinders
Rubber gloves
Rubber tubing
Strainers
Tempered glassware
Thermometers
Towels/sheets/
pillowcases
Hazards Associated with Methamphetamine
Laboratories
Explosions/Burns
An estimated 30% of clandestine laboratories are found after an
explosion or
fire.231 Patients injured in these incidents reportedly have
more severe inhalational injury, are more likely to require endotracheal
intubation, and spend a longer period on mechanical ventilation than case
controls.230,232-234 It has also been reported that these patients require
more fluid resuscitation that other burn patients, with estimates between
2 and 3 times the Parkland
formula.233,235 These patients also had higher
rates of pneumonia, respiratory failure, and sepsis when adjusted for
percentage involvement of total body surface area (TBSA), age, and
inhalational
injury.234 Agitation was also more common in the clandes-
tine-laboratory-related thermal burn patient than in case controls, requir-
ing higher doses of sedation and/or psychiatric
evaluation.233 Burns to the
face and eyes are
common.236
One study reported a 100% mortality rate for clandestine-laboratory-
related thermal burn patients with TBSA of 40% or more. Comparatively,
68
DM, February 2012
link to page 50 link to page 50 link to page 50 link to page 50 link to page 33 link to page 50 link to page 50 link to page 50 link to page 51 link to page 51
non-methamphetamine-related burn patients with TBSA of 60% or
greater are uniformly fatal. It has been theorized that the lower fatal
TBSA in clandestine-laboratory-related thermal burn patients may be due
to chemical injuries as well as toxicity from the methamphetamine
itself.235
Other characteristics of clandestine-laboratory-related thermal burn
patients are that they are more likely to be unemployed, uninsured, on
Medicare/Medicaid, or receiving some type of government assis-
tance.232,233,237 Treatment of these patients costs more than treatment of
other thermal burn patients, even after controlling for
TBSA.232,233
Chemical Injuries
Persons involved in clandestine methamphetamine manufacture may
also be injured by exposure to the chemicals used to manufacture
methamphetamine.232 The type and severity of chemical injury vary with
the substance and the route of exposure (eg, dermal absorption, inhala-
tion, ingestion).
Table 5 lists selected chemicals and their potential
hazards. Two substances that are commonly implicated in clandestine-
laboratory-related chemical injury are anhydrous ammonia and phosphine
gas.
The primary use of anhydrous ammonia is as a farm fertilizer. It is also
used in the Nazi/Birch method with an alkali metal to convert ephedrine
or pseudoephedrine into
methamphetamine.223,224 To obtain anhydrous
ammonia, methamphetamine manufacturers may steal it from storage
containers at farms and subsequently store it in propane
tanks.238
Clandestine-laboratory-related anhydrous ammonia injuries are reported
to involve higher TBSA, longer length of mechanical ventilation, and
longer inpatient stays and have a higher overall complication rate than
other anhydrous ammonia chemical
injuries.239 Injuries may be sustained,
not just by the manufacturers themselves, but also by others living in the
same household. Simulations of functional clandestine laboratories have
reported ammonia vapor concentrations that approached or exceeded
those deemed immediately dangerous to life and health, even at remote
sites within the
home.240,241
Anhydrous ammonia causes severe chemical injury to the skin, lungs,
and
eyes.242 Anhydrous ammonia is an alkali that quickly penetrates the
skin, causing liquefaction necrosis. Decontamination should be accom-
plished by copious irrigation. Dermal injury may require mechanical
debridement and skin grafting.
Pulmonary injury due to ammonia may be classified as acute or chronic,
depending on the nature of exposure. Acute pulmonary exposure occurs
DM, February 2012
69
link to page 50
TABLE 5. Hazards of selected chemicals found in clandestine
laboratories222,228,230
Acetic acid
Acute—eye irritation, airway inflammation, pulmonary edema,
severe burns, corneal ulcers, permanent eye damage;
chronic—upper airway irritation, eye irritation; flammable
when heated
Acetic anhydride
Vapors—eye, mucus membrane, and skin irritation; high
concentrations of vapors can lead to mucosal ulceration
and bronchospasm; liquid—immediate burning, corneal/
conjunctival edema, corneal opacification, vision loss, red
to white/wrinkled skin; skin burns may be delayed
Acetone
Eye, skin, and upper airway irritation; prolonged exposure—
coughing, blurry vision, tremors, seizures, stupor, bizarre
behavior, coma, death; flammable/explosive mixed with air
at room temperature; explosive when heated
Anhydrous ammonia
Burns to eyes, upper airway, and skin; conjunctivitis,
lacrimation, corneal irritation, blindness (temporary and
permanent); bronchospasm, wheezing, dyspnea, chest
pain, pulmonary edema, chemical pneumonitis
Benzaldehyde
Narcotic at moderate doses; induces seizure at higher
doses; eye and airway irritation; contact dermatitis; may be
absorbed through skin
Benzene
Acute—headache, dizziness, breathing difficulties, coughing,
pulmonary edema, coma, lung/liver/kidney damage, death;
chronic—irritation of eyes and airway, allergies, confusion,
short-term memory loss, bone marrow suppression, coma
death; flammable, may cause flash fires
Benzylchloride
Eye, mucus membrane, skin irritation; headache, lacrimation,
pulmonary edema, corneal injury, contact dermatitis
Ephedrine
Headache, hypertension, tachycardia, stroke; eye, lung, and
skin irritation
Ethanol
Inhalation—irritation or upper airway, headache
nausea/vomiting, drowsiness, confusion;
ingestion—confusion, dizziness, seizures, blurry vision,
blindness, coma, death; chronic—headache, decreased
coordination, nervous system/liver/stomach/heart damage
Ethyl ether
Headache, “drunkenness” vomiting; spontaneously explosive
in sunlight or oxygen or heat
Formic acid
Absorption through skin can cause systemic effects; severe,
painful burns, bloody diarrhea, pulmonary edema, shock,
death; explosive with contact of oxidizing agents
Freon
Eye irritation; vomiting, slurred speech, drunkenness, coma,
death; inhalation can cause sudden cardiac death
Hydriodic acid
Irritation of upper airways at low concentrations and dyspnea,
chest pain, bronchospasm, pneumonitis, pulmonary edema
at high concentrations; eye and skin irritation and burns
Hydrochloric acid/gas
Skin burns and allergies; inhalation may lead to pulmonary
(muriatic acid)
edema and permanent lung damage
Hypophosphorous acid
Burns especially to mucus membranes
Iodine
Vomiting, delirium, headache, hypotension, shock; mucus
membrane irritation, can lead to pulmonary edema; skin
irritation
70
DM, February 2012
TABLE 5. Continued
Lead acetate
Mostly a chronic exposure concern; abdominal pain, nausea/
vomiting, difficultly concentrating; increased exposure risk
to children due to developing nervous system
Lithium
Eye, skin, upper airway, and lung irritation; water-
reactive, generates hydrogen gas, explosive
Mercuric chloride
Acute—abdominal pain, vomiting, hematemesis, renal
failure; bizarre behavior, lung damage; chronic—
builds-up in brain/liver/kidneys; harmful fumes when
heated
Methanol
Eye and airway irritation; headache, nausea/vomiting,
abdominal pain, blindness, loss of consciousness,
damage to brain/pancreas/kidneys
Methylamine
Eye, mucus membrane, skin irritation; allergic or
chemical bronchitis; conjunctival hemorrhage,
superficial corneal opacities, corneal edema
Nitroethane
Eye, mucus membrane, skin irritation; nausea/vomiting/
diarrhea, mental status depression, ataxia, seizures
Petroleum distillates
Eye and skin irritation; delayed lung injury, depressed
mental status, seizures, loss of consciousness;
flammable mixed with air at room temperature
Phenyl-2-propanone (P2P)
Eye and skin irritation; nausea, headache, dizziness
Phenylacetic acid
Eye and skin irritation; nausea, headache, dizziness
Phosphine gas
Delayed pulmonary edema; dizziness, tremors, vomiting,
seizures; flammable, explosively reacts with air
Phosphoric acid
Eye, skin, and upper airway irritation; chronic—allergies,
lung/liver/bone marrow damage; releases phosphine
gas when contacts metal
Pseudoephedrine
Headache, hypertension, tachycardia, stroke; eye, lung,
and skin irritation
Pyridine
CNS depressant, liver/kidney damage, low back pain without
kidney damage, headache, nausea/vomiting, vertigo
Red phosphorous
If heated, produces yellow phosphorous (skin burns); if
heated with acid, produces phosphine gas
Sodium
Thermal and chemical skin burns; eye, mucus
membrane, lung, and skin irritation; water-reactive,
produces hydrogen gas and sodium hydroxide
Sodium hydroxide
Severe burns to eyes and skin; inhalation can lead to
burns in air passages; carcinogen; metal or fire
contact produces hydrogen gas
Sulfuric acid
Severe burns to eyes and skin; inhalation can lead to
lung damage, respiratory failure; chronic—lung/liver/
kidney damage, skin allergies; carcinogen; water-
reactive, produces harmful and corrosive fumes
Thorium oxide
Radioactive alpha emitter; carcinogen
Toluene
Inhalation—irritation or upper airway, headache nausea/
vomiting, drowsiness, confusion;
ingestion—confusion, dizziness, seizures, blurry
vision, blindness, coma, death
Trichloroethane
Eye, skin, upper airway, and lung irritation; pulmonary
edema, pneumonia, death; corneal damage
DM, February 2012
71
link to page 51 link to page 51 link to page 51 link to page 51 link to page 50 link to page 51 link to page 51 link to page 51 link to page 51 link to page 51 link to page 51
with the inhalation of high concentrations of ammonia vapor over a short
period (eg, ammonia discharge from a storage container) and is associated
with facial and upper airway
injury.243 Early intubation should be
undertaken because of the risk for glottis and supraglottic swelling
resulting in compromise of the airway.
Conversely, chronic pulmonary exposure because of exposure to lower
concentrations over a prolonged period (eg, ammonia fumes during
methamphetamine manufacture) is associated with injury throughout the
pulmonary tree. Chronic ammonia inhalational injury can be divided into
2 phases. The early phase is hallmarked by sloughing of pulmonary
epithelium resulting in hypoxia, edema, and airway obstruction. Aggres-
sive pulmonary toilet is necessary. The later phase presents with an initial
improvement in ventilation, followed by the gradual onset of fixed
obstruction that may be prolonged in nature. Bronchodilator and cortico-
steroid therapy may be of benefit, with antibiotics reserved for bacterial
superinfections.242
Ocular exposure may result in severe corneal injury. Immediate copious
irrigation should be instituted and the effectiveness of irrigation can be
monitored by serial measurements of the pH of ocular secretions.
Permanent vision loss from cataracts, atrophy of the iris, and acute angle
closure glaucoma are potential adverse effects associated with ammonia-
induced corneal injury. Corneal transplantation may be attempted; how-
ever, failure of transplantation secondary to scarring during the original
injury has been
reported.242
Phosphine gas is used as a grain fumigant, a precursor chemical, and a
chemical warfare
agent.244-246 Phosphine gas is a byproduct of illicit
methamphetamine manufacturing via the cold or red phosphorus
method.227 Phosphorous acid is formed when iodine and red phosphorus
are combined to form hydriodic acid and readily decomposes into
phosphine gas and phosphoric
acid.244 Heating of solutions containing
red phosphorus also produces phosphine
gas.240 During simulations of
functional clandestine laboratories, phosphine gas concentrations were
reported to exceed recommended upper limits of
exposure.247
Inhalational phosphine exposure causes irritant effects with dyspnea,
cough, delayed noncardiogenic pulmonary edema, ventilator-dependent
respiratory failure, and, in severe cases,
death.244-246 Exposure to phos-
phine gas may also result in ocular and dermal
irritation.245 A particularly
insidious aspect of phosphine gas exposure in clandestine laboratories are
case reports of law enforcement personnel being injured because of
phosphine gas exposure during
raids.248 Patients with suspected phos-
phine exposure should be observed for a 24-hour period to monitor for
72
DM, February 2012
link to page 51 link to page 51 link to page 51 link to page 51 link to page 51 link to page 50 link to page 51 link to page 50 link to page 51 link to page 51 link to page 51 link to page 51 link to page 52
delayed-onset pulmonary edema. Supplemental oxygen and mechanical
ventilation with positive end expiratory pressure may be necessary and
corticosteroids have been reported to be of benefit in animal
models.245
Phosphine exposure in workers exposed to phosphine in industrial
applications has been reported to result in prolonged pulmonary com-
plaints, including exertional dyspnea, decreased exercise tolerance, and
abnormal pulmonary function testing for years after exposure; these
symptoms were seen in patients with a history of tobacco use or
preexisting lung
diseases.245
Methamphetamine manufacturers are not the only persons who could be
harmed by the hazards present in clandestine laboratories. Other persons
living or working in the same building may be exposed to chemicals
involved in the manufacturing
process.240,241,247,249,250 First-respon-
ders and law enforcement personnel are also at risk for harm. First-
responders (eg, police or firefighters) may be particularly at risk if there
is no advance warning that caustic chemicals are present at a
site.251 The
appropriate use of personal protective equipment and training in the
recognition of clandestine laboratories is important in reducing risk for
these civil
servants.251 Clandestine laboratory investigators are at risk of
injury during the processing phase of a laboratory, where samples are
taken and chemicals are
removed.221 Hospital personnel are also at risk if
patients from clandestine laboratories are not appropriately identified and
decontaminated before entry into the
hospital.251 Symptoms reported by
first responders and law enforcement personnel include respiratory
irritation, dyspnea, headache, skin irritation/burns, mucous membrane
irritation, nausea/vomiting, and
dizziness.221,251
Pediatric Issues
In 17%-44% of discovered clandestine laboratories, children are living
in the same
building.252-255 Children may be exposed to chemicals used
in the manufacture of methamphetamine even if they are not in the
area where the methamphetamine is being produced, because of either
airborne
exposure
or
environmental
persistence
of
the
sub-
stances.240,241,247,249,250 Exposure can be to the methamphetamine
itself or to precursor chemicals or
solvents.256,257 Preschool children
are particularly at risk for exploratory ingestions due to hand-to-mouth
behavior and the significant portion of the day they spend in the
home.254,255 Improper storage of chemicals near food items or in
refrigerators increases the likelihood of pediatric
exposures.258 Environ-
mental persistence of chemicals following the manufacture of metham-
phetamine in kitchens or food preparation areas also puts children at risk
DM, February 2012
73
link to page 52 link to page 51 link to page 52 link to page 51 link to page 52 link to page 50 link to page 52
for
toxicity.259 Children living in buildings containing clandestine labo-
ratories are at risk for injury or death due to other nontoxicologic hazards:
lack of running water, improper maintenance of the building or building
contents, insect infestation, poor sanitation, booby-traps, loaded firearms,
and drug paraphernalia (eg, butane lighters, used hypodermic needles); all
may be present in buildings housing clandestine laboratories.
256,259,260
Parents or other adults may be more focused on manufacturing or using
methamphetamine than in child care, resulting in neglect, while chronic
abuse of methamphetamine may impair their judgment or hinder their
ability to care for
children.259,261 Protocols are useful in directing health
care providers in the assessment and treatment of these children. A
multidisciplinary approach involving health care providers, emergency
departments, social workers, law enforcement, and governmental children
services departments is likely to yield the best results, with the health and
physical safety of affected children being the utmost concern.
255,260-262
Environmental Contamination
For every pound of methamphetamine produced, it has been estimated
that up to 6 pounds of hazardous waste are generated.
258 Following the
seizure of a clandestine laboratory, extensive environmental remediation
may be necessary. Currently, extensive debate still exists regarding the
extent of remediation necessary and who is responsible for funding
it.222,231,263-265 Reported costs for environmental remediation vary from
$2000 to $100,000, depending on the size of the laboratory and the
practices of the
manufacturers.266 More research is necessary to deter-
mine the extent of remediation that must be performed and if there are any
long-term health or environmental effects related to former clandestine
methamphetamine laboratories and how these effects are moderated by
environmental remediation.
Conclusions
Methamphetamine abuse results in numerous adverse health effects,
including myocardial infarction, aortic dissection, pulmonary edema,
intracranial hemorrhage, ischemic stroke, mesenteric infarction, rhabdo-
myolysis with renal injury, necrotizing gingivostomatitis, psychiatric
disease, persistent cognitive impairment, sexually transmitted disease,
and transmission of blood-borne disease. Use in pregnant women has
been associated with fetal loss and perinatal maternal death. Metham-
phetamine increases the risk of traumatic death, which may be a result of
accident, suicide, or homicide.
74
DM, February 2012
Increases in methamphetamine abuse make methamphetamine a signif-
icant public health problem. Population morbidity and mortality, health
care costs, and law enforcement costs associated with methamphetamine
abuse are significant. Children living in clandestine laboratories or simply
in homes where methamphetamine is abused are at risk for abuse, neglect,
and toxicologic exposures.
The manufacture of methamphetamine also results in significant mor-
bidity and mortality because of thermal and blast injuries, caustic injury,
and other toxicologic exposures. Of additional concern is the risk posed
by these laboratories to first responders and law enforcement personnel.
Environmental persistence of hazardous waste generated by methamphet-
amine manufacture and the extent of necessary remediation efforts are
further important issues that continue to generate debate.
REFERENCES
1.
Hunt D, Kuck S, Truitt L. Methamphetamine Use: Lessons Learned. Cambridge,
MA: Abt Associates Inc., 2006 (Contract No. 209730)
2.
Cho AK, Segal DS. Amphetamine and Its Analogs: Psychopharmacology, Toxi-
cology, and Abuse. San Diego, CA: Academic Press, 1994.
3.
Leake CD. The Amphetamines: Their Actions and Uses. Springfield, IL: Thomas,
1958.
4.
Smith DE. Amphetamine Use, Misuse, and Abuse: Proceedings of the National
Amphetamine Conference, 1978. Boston, MA: G. K. Hall, 1979.
5.
Grinspoon L, Hedblom P. The Speed Culture: Amphetamine Use and Abuse in
America. Cambridge, MA: Harvard University Press, 1975.
6.
Rasmussen N. America’s first amphetamine Epidemic 1929-1971: A Quantitative
and Qualitative Retrospective with Implications for the Present. Am J Public Health
2008;98(6):974-85.
7.
Anglin MD, Burke C, Perrochet B, et al. History of the methamphetamine problem.
J Psychoact Drugs 2000;32(2):137-41.
8.
Mooney L, Rawson RA, Gonzales R. The methamphetamine Problem in the United
States. Annu Review Public Health 2010;31(1):385-98.
9.
Katzung BG, editor. Basic and Clinical Pharmacology, 8th ed. New York: Lange
Medical/McGraw-Hill, 2001.
10.
Nordahl TE, Salo R, Leamon M. Neuropsychological effects of chronic metham-
phetamine use on neurotransmitters and cognition: a review. J Neuropsychiatry
Clin Neurosci 2003;15(3):317-25.
11.
Goldstein DS, Nurnberger Jr, J Simmons S, et al. Effects of injected sympathomi-
metic amines on plasma catecholamines and circulatory variables in man. Life Sci
1983;32(10):1057-63.
12.
Kish SJ. Pharmacologic mechanisms of crystal meth [see comment]. CMAJ
2008;178(13):1679-82.
13.
Volz TJ, Hanson GR, Fleckenstein AE. The role of the plasmalemmal dopamine
and vesicular monoamine transporters in methamphetamine-induced dopaminergic
deficits. J Neurochem 2007;101(4):883-8.
DM, February 2012
75
14.
Brown JM, Hanson GR, Fleckenstein AE. Methamphetamine rapidly decreases
vesicular dopamine uptake. J Neurochem 2000;74(5):2221-3.
15.
Brown JM, Hanson GR, Fleckenstein AE. Cocaine-induced increases in vesicular
dopamine uptake: role of dopamine receptors. J Pharmacol Exp Ther 2001;298
(3):1150-3.
16.
Sandoval V, Riddle EL, Hanson GR, et al. Methylphenidate redistributes vesicular
monoamine transporter-2: role of dopamine receptors. J Neurosci 2002;22(19):
8705-10.
17.
Hogan KA, Staal RG, Sonsalla PK. Analysis of VMAT2 binding after metham-
phetamine or MPTP treatment: disparity between homogenates and vesicle prepa-
rations. J Neurochem 2000;74(5):2217-20.
18.
Fleckenstein AE, Volz TJ, Riddle EL, et al. New insights into the mechanism of
action of amphetamines. Annu Rev Pharmacol Toxicol 2007;47:681-98.
19.
Riddle EL, Topham MK, Haycock JW, et al. Differential trafficking of the vesicular
monoamine transporter-2 by methamphetamine and cocaine. Eur J Pharmacol
2002;449(1-2):71-4.
20.
Cervinski MA, Foster JD, Vaughan RA. Psychoactive substrates stimulate dopa-
mine transporter phosphorylation and down-regulation by cocaine-sensitive and
protein kinase C-dependent mechanisms. J Biol Chem 2005;280(49):40442-9.
21.
Baucum AJ 2nd, Rau KS, Riddle EL, et al. Methamphetamine increases dopamine
transporter higher molecular weight complex formation via a dopamine- and
hyperthermia-associated mechanism. J Neurosci 2004;24(13):3436-43.
22.
Sorkina T, Doolen S, Galperin E, et al. Oligomerization of dopamine transporters
visualized in living cells by fluorescence resonance energy transfer microscopy.
J Biol Chem 2003;278(30):28274-83.
23.
Schenk JO. The functioning neuronal transporter for dopamine: kinetic mechanisms
and effects of amphetamines, cocaine and methylphenidate. Prog Drug Res 2002;
59:111-31.
24.
Kahlig KM, Binda F, Khoshbouei H, Blakely RD, McMahon DG, Javitch JA, et al.
Amphetamine induces dopamine efflux through a dopamine transporter channel.
Proc Natl Acad Sci USA 2005;102(9):3495-500.
25.
Jones SR, Gainetdinov RR, Wightman RM, et al. Mechanisms of amphetamine
action revealed in mice lacking the dopamine transporter. J Neurosci 1998;18(6):
1979-86.
26.
Sulzer D, Rayport S. Amphetamine and other psychostimulants reduce pH
gradients in midbrain dopaminergic neurons and chromaffin granules: a mechanism
of action. Neuron 1990;5(6):797-808.
27.
Cadet JL, Jayanthi S, Deng X. Speed kills: cellular and molecular bases of
methamphetamine-induced nerve terminal degeneration and neuronal apoptosis.
FASEB J 2003;17(13):1775-88.
28.
Wilson JM, Kalasinsky KS, Levey AI, et al. Striatal dopamine nerve terminal
markers in human, chronic methamphetamine users. Nat Med 1996;2(6):699-703.
29.
Volkow ND, Chang L, Wang GJ, et al. Association of dopamine transporter
reduction with psychomotor impairment in methamphetamine abusers. Am J
Psychiatry 2001;158(3):377-82.
30.
McCann UD, Wong DF, Yokoi F, et al. Reduced striatal dopamine transporter
density in abstinent methamphetamine and Methcathinone users: evidence from
76
DM, February 2012
positron emission tomography studies with [11C]WIN-35,428. J Neurosci
1998;18(20):8417-22.
31.
Volkow ND, Chang L, Wang GJ, et al. Loss of dopamine transporters in
methamphetamine abusers recovers with protracted abstinence. J Neurosci
2001;21(23):9414-8.
32.
Sung YH, Cho SC, Hwang J, et al. Relationship between N-acetyl-aspartate in gray
and white matter of abstinent methamphetamine abusers and their history of drug
abuse: a proton magnetic resonance spectroscopy study. Drug Alcohol Depend
2007;88(1):28-35.
33.
Kim SJ, Lyoo IK, Hwang J, et al. Prefrontal grey-matter changes in short-term and
long-term abstinent methamphetamine abusers. Int J Neuropsychopharmacol
2006;9(2):221-8.
34.
Nordahl TE, Salo R, Natsuaki Y, et al. Methamphetamine users in sustained
abstinence: a proton magnetic resonance spectroscopy study. Arch Gen Psychiatry
2005;62(4):444-52.
35.
Nordahl TE, Salo R, Possin K, et al. Low N-acetyl-aspartate and high choline in the
anterior cingulum of recently abstinent methamphetamine-dependent subjects: a
preliminary proton MRS study. Magnetic resonance spectroscopy. Psychiatry Res
2002;116(1-2):43-52.
36.
Ernst T, Chang L, Leonido-Yee M, et al. Evidence for long-term neurotoxicity
associated with methamphetamine abuse: A 1H MRS study. Neurology 2000;
54(6):1344-9.
37.
Marshall JF, Belcher AM, Feinstein EM, et al. Methamphetamine-induced neural
and cognitive changes in rodents. Addiction 2007;102(Suppl 1):61-9.
38.
Thomas DM, Francescutti-Verbeem DM, Kuhn DM. The newly synthesized pool
of dopamine determines the severity of methamphetamine-induced neurotoxicity.
J Neurochem 2008;105(3):605-16.
39.
Kita T, Takeshima M, Wagner GC, et al. [New perspectives on the mechanism of
methamphetamine-induced neurotoxicity]. Nihon Shinkei Seishin Yakurigaku
Zasshi 2008;28(2):49-61.
40.
Kita T, Wagner GC, Nakashima T. Current research on methamphetamine-induced
neurotoxicity: animal models of monoamine disruption. J Pharmacol Sci 2003;92
(3):178-95.
41.
Kita T, Nakashima T. [A recent trend in methamphetamine-induced neurotoxicity].
Nihon Shinkei Seishin Yakurigaku Zasshi 2002;22(2):35-47.
42.
Imam SZ, el-Yazal J, Newport GD, et al. Methamphetamine-induced dopami-
nergic neurotoxicity: role of peroxynitrite and neuroprotective role of antioxi-
dants
and
peroxynitrite
decomposition
catalysts.
Ann
NY
Acad
Sci
2001;939:366-80.
43.
Imam SZ, Ali SF. Selenium, an antioxidant, attenuates methamphetamine-
induced dopaminergic toxicity and peroxynitrite generation. Brain Res 2000;
855(1):186-91.
44.
Itzhak Y, Gandia C, Huang PL, et al. Resistance of neuronal nitric oxide
synthase-deficient mice to methamphetamine-induced dopaminergic neurotoxicity.
J Pharmacol Exp Ther 1998;284(3):1040-7.
45.
Imam SZ, Ali SF. Aging increases the susceptiblity to methamphetamine-induced
dopaminergic neurotoxicity in rats: correlation with peroxynitrite production and
hyperthermia. J Neurochem 2001;78(5):952-9.
DM, February 2012
77
46.
Miller DB, O’Callaghan JP, Ali SF. Age as a susceptibility factor in the striatal
dopaminergic neurotoxicity observed in the mouse following substituted amphet-
amine exposure. Ann NY Acad Sci 2000;914:194-207.
47.
Chung A, Lyoo IK, Kim SJ, et al. Decreased frontal white-matter integrity in
abstinent methamphetamine abusers. Int J Neuropsychopharmacol 2007;10(6):
765-75.
48.
Kim SJ, Lyoo IK, Hwang J, Sung YH, Lee HY, Lee DS, et al. Frontal glucose
hypometabolism in abstinent methamphetamine users. Neuropsychopharmacology
2005;30(7):1383-91.
49.
He SY, Matoba R, Fujitani N, et al. Cardiac muscle lesions associated with chronic
administration of methamphetamine in rats. Am J Forensic Med Pathol 1996;
17(2):155-62.
50.
He SY, Matoba R, Sodesaki K, et al. Morphological and morphometric investiga-
tion of cardiac lesions after chronic administration of methamphetamine in rats.
Nihon Hoigaku Zasshi 1996;50(2):63-71.
51.
Kaiho M, Ishiyama I. Morphological study of acute myocardial lesions experimen-
tally induced by methamphetamine. Nihon Hoigaku Zasshi 1989;43(6):460-8.
52.
Maeno Y, Iwasa M, Inoue H, et al. Direct effects of methamphetamine on
hypertrophy and microtubules in cultured adult rat ventricular myocytes. Forensic
Sci Int 2000;113(1-3):239-43.
53.
He SY. Methamphetamine-induced toxicity in cultured adult rat cardiomyocytes.
Nihon Hoigaku Zasshi 1995;49(3):175-86.
54.
Maeno Y, Iwasa M, Inoue H, et al. Methamphetamine induces an increase in cell
size and reorganization of myofibrils in cultured adult rat cardiomyocytes. Int J Leg
Med 2000;113(4):201-7.
55.
Matoba R. [Cardiac lesions in methamphetamine abusers]. Nihon Hoigaku Zasshi
2001;55(3):321-30.
56.
Islam MN, Jesmine K, Kong Sn Molh A, et al. Histopathological studies of cardiac
lesions after long term administration of methamphetamine in high dosage—Part II.
Leg Med (Tokyo) 2009;11(Suppl 1):S147-50.
57.
Yi SH, Ren L, Yang TT, et al. Myocardial lesions after long-term administration of
methamphetamine in rats. Chin Med Sci J 2008;23(4):239-43.
58.
Richards JR, Bretz SW, Johnson EB, et al. Methamphetamine abuse and emergency
department utilization. West J Med 1999;170(4):198-202.
59.
Newton TF, De La Garza 2nd, R Kalechstein AD, et al. Cocaine and methamphet-
amine produce different patterns of subjective and cardiovascular effects. Pharma-
col Biochem Behav 2005;82(1):90-7.
60.
Wijetunga M, Bhan R, Lindsay J, et al. Acute coronary syndrome and crystal
methamphetamine use: a case series. Hawaii Med J 2004;63(1):8-13, 25.
61.
Turnipseed SD, Richards JR, Kirk JD, et al. Frequency of acute coronary syndrome
in patients presenting to the emergency department with chest pain after metham-
phetamine use. J Emerg Med 2003;24(4):369-73.
62.
Farnsworth TL, Brugger CH, Malters P. Myocardial infarction after intranasal
methamphetamine. Am J Health Syst Pharm 1997;54(5):586-7.
63.
Chen JP. Methamphetamine-associated acute myocardial infarction and cardio-
genic shock with normal coronary arteries: refractory global coronary microvas-
cular spasm. J Invasive Cardiol 2007;19(4):E89-92.
78
DM, February 2012
64.
Karch SB, Stephens BG, Ho CH. Methamphetamine-related deaths in San
Francisco: demographic, pathologic, and toxicologic profiles. J Forensic Sci 1999;
44(2):359-68.
65.
Hong R, Matsuyama E, Nur K. Cardiomyopathy associated with the smoking of
crystal methamphetamine. JAMA 1991;265(9):1152-4.
66.
Haning W, Goebert D. Electrocardiographic abnormalities in methamphetamine
abusers. Addiction 2007;102(Suppl 1):70-5.
67.
Wijetunga M, Seto T, Lindsay J, et al. Crystal methamphetamine-associated
cardiomyopathy: tip of the iceberg? J Toxicol Clin Toxicol 2003;41(7):
981-6.
68.
Nestor TA, Tamamoto WI, Kam TH, et al. Acute pulmonary oedema caused by
crystalline methamphetamine. Lancet 1989;2(8674):1277-8.
69.
Jacobs LJ. Reversible dilated cardiomyopathy induced by methamphetamine. Clin
Cardiol 1989;12(12):725-7.
70.
Srikanth S, Barua R, Ambrose J. Methamphetamine-associated acute left ventric-
ular dysfunction: a variant of stress-induced cardiomyopathy. Cardiology 2008;
109(3):188-92.
71.
Wako E, LeDoux D, Mitsumori L, et al. The emerging epidemic of methamphet-
amine-induced aortic dissections. J Cardiovasc Surg 2007;22(5):390-3.
72.
Swalwell CI, Davis GG. Methamphetamine as a risk factor for acute aortic
dissection. J Forensic Sci 1999;44(1):23-6.
73.
Davis GG, Swalwell CI. Acute aortic dissections and ruptured berry aneurysms
associated with methamphetamine abuse. Forensic J 1994;39(6):1481-5.
74.
Takasaki T, Nishida N, Esaki R, et al. Unexpected death due to right-sided infective
endocarditis in a methamphetamine abuser. Leg Med 2003;5(1):65-8.
75.
Hiroshi K, Akira K, Minori N, et al. An autopsy case of infectious endocarditis in
a methamphetamine abuser usefulness of microbiological examination. Soud Lek
2005;50(2):18-22.
76.
Bergstrom KG. Cutaneous clues to drug addiction. J Drugs Dermatol 2008;
7(3):303-5.
77.
Marschall MA, Dolezal RF, Cohen M, et al. Chronic wounds and delusions of
parasitosis in the drug abuser. Plast Reconstr Surg 1991;88(2):328-30.
78.
Morb M. Methamphetamine use and HIV risk behaviors among heterosexual
men—preliminary results from five northern California counties, December 2001-
November 2003. MMWR Morb Mort Wkly Rep 2006;55(10):273-7.
79.
Molitor F, Truax SR, Ruiz JD, et al. Association of methamphetamine use during
sex with risky sexual behaviors and HIV infection among non-injection drug users.
West J Med 1998;168(2):93-7.
80.
Copeland AL, Sorensen JL. Differences between methamphetamine users and
cocaine users in treatment. Drug Alcohol Depend 2001;62(1):91-5.
81.
Ogasawara K, Ogawa A, Kita H, et al. [Intracerebral hemorrhage and characteristic
angiographic changes associated with methamphetamine—a case report]. No
Shinkei 1986;38(10):967-71.
82.
Shibata S, Mori K, Sekine I, et al. Subarachnoid and intracerebral hemorrhage
associated with necrotizing angiitis due to methamphetamine abuse—an autopsy
case. Neurol Med Chir 1991;31(1):49-52.
83.
Citron BP, Halpern M, McCarron M, et al. Necrotizing angiitis associated with
drug abuse. N Engl J Med 1970;283(19):1003-11.
DM, February 2012
79
84.
Bingham C, Beaman M, Nicholls AJ, et al. Necrotizing renal vasculopathy
resulting in chronic renal failure after ingestion of methamphetamine and 3,4-
methylenedioxymethamphetamine (“ecstasy”). Nephrol Dial Transplant 1998;
13(10):2654-5.
85.
Gonzales R, Marinelli-Casey P, Hillhouse M, et al. Hepatitis A and B infection
among methamphetamine-dependent users. J Subst Abus Treat 2008;35(3):351-2.
86.
Scheinmann R, Hagan H, Lelutiu-Weinberger C, et al. Non-injection drug use and
hepatitis C virus: a systematic review. Drug Alcohol Depend 2007;89(1):1-12.
87.
Howe CJ, Fuller CM, Ompad DC, et al. Association of sex, hygiene and drug
equipment sharing with hepatitis C virus infection among non-injecting drug users
in New York City. Drug Alcohol Depend 2005;79(3):389-95.
88.
Kamijo Y, Soma K, Nishida M, et al. Acute liver failure following intravenous
methamphetamine. Vet Hum Toxicol 2002;44(4):216-7.
89.
Roberts SM, Harbison RD, James RC. Methamphetamine potentiation of carbon
tetrachloride hepatotoxicity in mice. J Pharmacol Exp Ther 1994;271(2):1051-7.
90.
Roberts SM, Harbison RD, James RC. Mechanistic studies on the potentiation of
carbon tetrachloride hepatotoxicity by methamphetamine. Toxicology 1995;97
(1-3):49-57.
91.
Brannan TA, Soundararajan S, Houghton BL. Methamphetamine-associated shock
with intestinal infarction. MedGenMed 2004;6(4):6.
92.
Johnson TD, Berenson MM. Methamphetamine-induced ischemic colitis. J Clin
Gastroenterol 1991;13(6):687-9.
93.
Cappell MS. Colonic toxicity of administered drugs and chemicals. Am J
Gastroenterol 2004;99(6):1175-90.
94.
Kelly MA, Gorelick PB, Mirza D. The role of drugs in the etiology of stroke. Clin
Neuropharmacol 1992;15(4):249-75.
95.
Dirkx CA, Gerscovich EO. Sonographic findings in methamphetamine-induced
ischemic colitis. J Clin Ultrasound 1998;26(9):479-82.
96.
Ito Y, Jono H, Shojo H. A histopathological study of pancreatic lesions after
chronic administration of methamphetamine to rats. Kurume Med J 1997;44
(3):209-15.
97.
Ito Y, Jono H, Shojo H. Ultrastructural findings of the endothelial cells in
pancreatic lesions after chronic administration of methamphetamine in rats.
Kurume Med J 1998;45(3):243-6.
98.
Kurtz SP. Post-circuit blues: motivations and consequences of crystal meth use
among gay men in Miami. Aids Behav 2005;9(1):63-72.
99.
Semple SJ, Patterson TL, Grant I. A comparison of injection and non-injection
methamphetamine-using HIV positive men who have sex with men. Drug Alcohol
Depend 2004;76(2):203-12.
100.
Shoptaw S, Peck J, Reback CJ, et al. Psychiatric and substance dependence
comorbidities, sexually transmitted diseases, and risk behaviors among metham-
phetamine-dependent gay and bisexual men seeking outpatient drug abuse treat-
ment. J Psychoact Drugs 2003;35(Suppl 1):161-8.
101.
Beyrer C, Razak MH, Jittiwutikarn J, et al. Methamphetamine users in northern
Thailand: changing demographics and risks for HIV and STD among treatment-
seeking substance abusers. Int J STD AIDS 2004;15(10):697-704.
102.
Q&A. Brush Up on the Facts about Meth Mouth, 2007; Available from:
http://www.drugfree.org/Portal/DrugIssue/MethResources/meth_mouth.html.
80
DM, February 2012
103.
PBS. FRONTLINE: the Meth Epidemic: How Meth Destroys the Body, 2009;
Available from:
http://www.pbs.org/wgbh/pages/frontline/meth/body/.
104.
Goodchild JH, Donaldson M, Mangini DJ. Methamphetamine abuse and the impact
on dental health. Dent Today 2007;26(5):124, 126, 128-31; [Quiz] 131.
105.
Klasser GD, Epstein JB. The methamphetamine epidemic and dentistry. Gen Dent
2006;54(6):431-9 [Quiz 440-8].
106.
Shaner JW. Caries associated with methamphetamine abuse. J Mich Dent Assoc
2002;84(9):42-7.
107.
Padilla R, Ritter AV. Meth mouth: methamphetamine and oral health. J Esthet
Restor Dent 2008;20(2):148-9.
108.
Cretzmeyer M, Walker J, Hall JA, et al. Methamphetamine use and dental disease:
results of a pilot study. J Dent Child (Chic) 2007;74(2):85-92.
109.
Richards JR, Johnson EB, Stark RW, et al. Methamphetamine abuse and rhabdo-
myolysis in the ED: a 5-year study. Am J Emerg Med 1999;17(7):681-5.
110.
Swanson SM, Sise CB, Sise MJ, et al. The scourge of methamphetamine: impact on
a level I trauma center. J Trauma 2007;63(3):531-7.
111.
Tominaga GT, Garcia G, Dzierba A, et al. Toll of methamphetamine on the trauma
system. Arch Surg 2004;139(8):844-7.
112.
Hadjizacharia P, Green DJ, Plurad D, et al. Methamphetamines in trauma: effect on
injury patterns and outcome. J Trauma 2009;66(3):895-8.
113.
Banooni P, Rickman LS, Ward DM. Pott puffy tumor associated with intranasal
methamphetamine. JAMA 2000;283(10):1293.
114.
Inamasu J, Nakamura Y, Saito R, et al. Subcortical hemorrhage caused by
methamphetamine abuse: efficacy of the triage system in the differential diagno-
sis— case report. Neurol Med Chir 2003;43(2):82-4.
115.
Davis GG, Swalwell CI. The incidence of acute cocaine or methamphetamine
intoxication in deaths due to ruptured cerebral (berry) aneurysms. J Forensic Sci
1996;41(4):626-8.
116.
Miyashita T, Hayashi T, Ishida Y, et al. A fatal case of pontine hemorrhage related
to methamphetamine abuse. J Forensic Leg Med 2007;14(7):444-7.
117.
Shibata S, Mori K, Sekine I, et al. [An autopsy case of subarachnoid and
intracerebral hemorrhage and necrotizing angitis associated with methamphetamine
abuse]. No Shinkei 1988;40(11):1089-94.
118.
Beránková K, Habrdová V, Balíková M, et al. Methamphetamine in hair and
interpretation of forensic findings in a fatal case. Forensic Sci Int 2005;153(1):
93-7.
119.
Yen DJ, Wang SJ, Ju TH, et al. Stroke associated with methamphetamine
inhalation. Eur Neurol 1994;34(1):16-22.
120.
Moriya F, Hashimoto Y. A case of fatal hemorrhage in the cerebral ventricles
following intravenous use of methamphetamine. Forensic Sci Int 2002;129
(2):104-9.
121.
Perez Jr, JA Arsura EL, Strategos S. Methamphetamine-related stroke: four cases.
J Emerg Med 1999;17(3):469-71.
122.
Rothrock JF, Rubenstein R, Lyden PD. Ischemic stroke associated with metham-
phetamine inhalation. Neurology 1988;38(4):589-92.
123.
Sachdeva K, Woodward KG. Caudal thalamic infarction following intranasal
methamphetamine use. Neurology 1989;39(2 Pt 1):305-6.
DM, February 2012
81
124.
Minabe Y, Emori K, Kurachi M. Effects of chronic treatment of methamphetamine
and imipramine on amygdaloid seizure’s generation. Jpn J Psychiatry Neurol
1988;42(2):337-43.
125.
Simon SL, Domier C, Carnell J, et al. Cognitive impairment in individuals currently
using methamphetamine. Am J Addict 2000;9(3):222-31.
126.
Moon M, Do KS, Park J, et al. Memory impairment in methamphetamine
dependent patients. Int J Neurosci 2007;117(1):1-9.
127.
Kirkpatrick MG, Metcalfe J, Greene MJ, et al. Effects of intranasal methamphet-
amine on metacognition of agency. Psychopharmacol Berl 2008;197(1):137-44.
128.
Kalechstein AD, Newton TF, Green M. Methamphetamine dependence is associ-
ated with neurocognitive impairment in the initial phases of abstinence. J Neuro-
psychiatry Clin Neurosci 2003;15(2):215-20.
129.
Salo R, Nordahl TE, Natsuaki Y, et al. Attentional control and brain metabolite
levels in methamphetamine abusers. Biol Psychiatry 2007;61(11):1272-80.
130.
Salo R, Nordahl TE, Buonocore MH, et al. Cognitive control and white matter
callosal microstructure in methamphetamine-dependent subjects: a diffusion tensor
imaging study. Biol Psychiatry 2009;65(2):122-8.
131.
Cherner M, Letendre S, Heaton RK, et al. Hepatitis C augments cognitive deficits
associated with HIV infection and methamphetamine. Neurology 2005;64(8):
1343-7.
132.
Chana G, Everall IP, Crews L, et al. Cognitive deficits and degeneration of
interneurons in HIV⫹ methamphetamine users. Neurology 2006;67(8):1486-9.
133.
Chang L, Ernst T, Speck O, et al. Additive effects of HIV and chronic metham-
phetamine use on brain metabolite abnormalities. Am J Psychiatry 2005;162
(2):361-9.
134.
Taylor MJ, Schweinsburg BC, Alhassoon OM, et al. Effects of human immuno-
deficiency virus and methamphetamine on cerebral metabolites measured with
magnetic resonance spectroscopy. J Neurovirol 2007;13(2):150-9.
135.
Cai NS, Cadet JL. The combination of methamphetamine and of the HIV protein,
Tat, induces death of the human neuroblastoma cell line, SH-SY5Y. Synapse
2008;62(7):551-2.
136.
Cadet JL, Krasnova IN. Interactions of HIV and methamphetamine: cellular and
molecular mechanisms of toxicity potentiation. Neurotox Res 2007;12(3):181-
204.
137.
Theodore S, Cass WA, Nath A, et al. Progress in understanding basal ganglia
dysfunction as a common target for methamphetamine abuse and HIV-1 neurode-
generation. Curr HIV Res 2007;5(3):301-13.
138.
Sperling LS, Horowitz JL. Methamphetamine-induced choreoathetosis and rhab-
domyolysis. Ann Intern Med 1994;121(12):986.
139.
Rhee KJ, Albertson TE, Douglas JC. Choreoathetoid disorder associated with
amphetamine-like drugs. Am J Emerg Med 1988;6(2):131-3.
140.
Buffum JC, Shulgin AT. Overdose of 2.3 grams of intravenous methamphetamine:
case, analysis and patient perspective. J Psychoact Drugs 2001;33(4):409-12.
141.
Wijaya J, Salu P, Leblanc A, et al. Acute unilateral visual loss due to a single
intranasal methamphetamine abuse. Bull Soc Belge Ophtalmol 1999;271:19-25.
142.
Shaw HE Jr, Lawson JG, Stulting RD. Amaurosis fugax and retinal vasculitis
associated with methamphetamine inhalation. J Clin Neuro Ophthalmol 1985;
5(3):169-76.
82
DM, February 2012
143.
Nakatani Y, Hara T. Disturbance of consciousness due to methamphetamine abuse.
A study of 2 patients. Psychopathology 1998;31(3):131-7.
144.
Newton TF, Kalechstein AD, Duran S, et al. Methamphetamine abstinence
syndrome: preliminary findings. Am J Addict 2004;13(3):248-55.
145.
Kalechstein AD, Newton TF, Longshore D, et al. Psychiatric comorbidity of
methamphetamine dependence in a forensic sample. J Neuropsychiatry Clin
Neurosci 2000;12(4):480-4.
146.
Zweben JE, Cohen JB, Christian D, et al. Psychiatric symptoms in methamphet-
amine users. Am J Addict 2004;13(2):181-90.
147.
Yen C-F, Shieh B-L. Suicidal ideation and correlates in Taiwanese adolescent
methamphetamine users. J Nerv Ment Dis 2005;193(7):444-9.
148.
Darke S, Kaye S, McKetin R, et al. Major physical and psychological harms of
methamphetamine use Drug Alcohol Rev 2008;27(3):253– 62.
149.
Callor WB, Petersen E, Gray D, et al. Preliminary findings of noncompliance with
psychotropic medication and prevalence of methamphetamine intoxication associ-
ated with suicide completion. Crisis 2005;26(2):78 – 84.
150.
Chen C-K, Lin S-K, Huang M-C, et al. Analysis of association of clinical correlates
and 5-HTTLPR polymorphism with suicidal behavior among Chinese methamphet-
amine abusers Psychiatry Clin Neurosci 2007;61(5):479 – 86.
151.
Glasner-Edwards S, Mooney LJ, Marinelli-Casey P, et al. Risk factors for suicide
attempts in methamphetamine-dependent patients. Am J Addict 2008;17(1):24-7.
152.
Kratofil PH, Baberg HT, Dimsdale JE. Self-mutilation and severe self-injurious
behavior associated with amphetamine psychosis. Gen Hosp Psychiatry 1996;
18(2):117-20.
153.
Israel JA, Lee K. Amphetamine usage and genital self-mutilation. Addiction
2002;97(9):1215-8.
154.
McKetin R, McLaren J, Lubman DI, et al. Hostility among methamphetamine users
experiencing psychotic symptoms. Am J Addict 2008;17(3):235-40.
155.
Chen CK, Lin SK, Sham PC, et al. Pre-morbid characteristics and co-morbidity of
methamphetamine users with and without psychosis. Psychol Med 2003;33
(8):1407-14.
156.
Srisurapanont M, Ali R, Marsden J, et al. Psychotic symptoms in methamphetamine
psychotic in-patients. Int J Neuropsychopharmacol 2003;6(4):347-52.
157.
Pasic J, Russo JE, Ries RK, et al. Methamphetamine users in the psychiatric
emergency services: a case-control study. Am J Drug Alcohol Abus 2007;33
(5):675-86.
158.
Jacobs E, Fujii D, Schiffman J, et al. An exploratory analysis of neurocognition in
methamphetamine-induced psychotic disorder and paranoid schizophrenia. Cogn
Behav Neurol 2008;21(2):98-103.
159.
McKetin R, McLaren J, Lubman DI, et al. The prevalence of psychotic symptoms
among methamphetamine users. Addiction 2006;101(10):1473-8.
160.
Farrell M, Marsden J, Ali R, et al. Methamphetamine: drug use and psychoses
becomes a major public health issue in the Asia Pacific region. Addiction
2002;97(7):771-2.
161.
Ujike H, Sato M. Clinical features of sensitization to methamphetamine observed
in patients with methamphetamine dependence and psychosis. Ann NY Acad Sci
2004;1025:279-87.
DM, February 2012
83
162.
Yui K, Ikemoto S, Ishiguro T, et al. Studies of amphetamine or methamphetamine
psychosis in Japan: relation of methamphetamine psychosis to schizophrenia. Ann
NY Acad Sci 2000;914:1-12.
163.
Iwanami A, Sugiyama A, Kuroki N, et al. Patients with methamphetamine
psychosis admitted to a psychiatric hospital in Japan. A preliminary report. Acta
Psychiatr Scand 1994;89(6):428-32.
164.
Fujii D. Risk factors for treatment-resistive methamphetamine psychosis. J Neu-
ropsychiatry Clin Neurosci 2002;14(2):239-40.
165.
Sekine Y, Minabe Y, Kawai M, et al. Metabolite alterations in basal ganglia
associated with methamphetamine-related psychiatric symptoms. A proton MRS
study. Neuropsychopharmacology 2002;27(3):453-61.
166.
Chin KM, Channick RN, Rubin LJ. Is methamphetamine use associated with
idiopathic pulmonary arterial hypertension? Chest 2006;130(6):1657-63.
167.
Kneehans S, Sziegoleit W, Krause M, et al. [Clinical-pharmacological studies on
the effect of mephentermine and methamphetamine on the hemodynamics of the
lung circulation]. Z Gesamte Inn Med 1975;30(6):227-30.
168.
Schaiberger PH, Kennedy TC, Miller FC, et al. Pulmonary hypertension associated
with long-term inhalation of “crank” methamphetamine. Chest 1993;104(2):614-6.
169.
Rothman RB, Baumann MH. Methamphetamine and idiopathic pulmonary arterial
hypertension: role of the serotonin transporter. Chest 2007;132(4):1412-3.
170.
Thompson CA. Pulmonary arterial hypertension seen in methamphetamine abusers.
Am J Health Syst Pharm 2008;65(12):1109-10.
171.
Arria AM, Derauf C, Lagasse LL, et al. Methamphetamine and other substance use
during pregnancy: preliminary estimates from the Infant Development, Environ-
ment, and Lifestyle (IDEAL) study. Matern Child Health J 2006;10(3):293-302.
172.
Smith LM, LaGasse LL, Derauf C, et al. The infant development, environment, and
lifestyle study: effects of prenatal methamphetamine exposure, polydrug exposure,
and poverty on intrauterine growth. Pediatrics 2006;118(3):1149-56.
173.
Little BB, Snell LM, Gilstrap 3rd. LC Methamphetamine abuse during pregnancy:
outcome and fetal effects. Obstet Gynecol 1988;72(4):541-4.
174.
Oro AS; Dixon SD. Perinatal cocaine and methamphetamine exposure: maternal
and neonatal correlates. J Pediatr 1987;111(4):571-8.
175.
Dixon SD, Bejar R. Echoencephalographic findings in neonates associated with
maternal cocaine and methamphetamine use: incidence and clinical correlates.
J Pediatr 1989;115(5 Pt 1):770-8.
176.
Stewart JL, Meeker JE. Fetal and infant deaths associated with maternal metham-
phetamine abuse. J Anal Toxicol 1997;21(6):515-7.
177.
Chomchai C, Na Manorom N, Watanarungsan P, et al. Methamphetamine abuse
during pregnancy and its health impact on neonates born at Siriraj Hospital,
Bangkok, Thailand. Southeast Asian J Trop Med Public Health 2004;35(1):228-31.
178.
Smith LM, Lagasse LL, Derauf C, et al. Prenatal methamphetamine use and
neonatal neurobehavioral outcome. Neurotoxicol Teratol 2008;30(1):20-8.
179.
Paz MS, Smith LM, LaGasse LL, et al. Maternal depression and neurobehavior in
newborns prenatally exposed to methamphetamine. Neurotoxicol Teratol 2009;31
(3):177-82.
180.
Dahshan A. Prenatal exposure to methamphetamine presenting as neonatal choles-
tasis. J Clin Gastroenterol 2009;43(1):88-90.
84
DM, February 2012
181.
Chang L, Alicata D, Ernst T, et al. Structural and metabolic brain changes in the
striatum associated with methamphetamine abuse. Addiction 2007;102(Suppl
1):16-32.
182.
Chang L, Smith LM, LoPresti C, et al. Smaller subcortical volumes and cognitive
deficits in children with prenatal methamphetamine exposure. Psychiatry Res
2004;132(2):95-106.
183.
Melo P, Moreno VZ, Vázquez SP, et al. Myelination changes in the rat optic nerve
after prenatal exposure to methamphetamine. Brain Res 2006;1106(1):21-9.
184.
Slamberová R, Bernásková K, Matejovská I, et al. Does prenatal methamphetamine
exposure affect seizure susceptibility in adult rats with acute administration of the
same drug? Epilepsy Res 2008;78(1):33-9.
185.
Slamberová R, Pometlová M, Charousová P. Postnatal development of rat pups is
altered by prenatal methamphetamine exposure. Prog Neuropsychopharmacol Biol
Psychiatry 2006;30(1):82-8.
186.
Slamberová R, Pometlová M, Rokyta R. Effect of methamphetamine exposure
during prenatal and preweaning periods lasts for generations in rats. Dev Psycho-
biol 2007;49(3):312-22.
187.
Yamamoto Y, Yamamoto K, Fukui Y, et al. Teratogenic effects of methamphet-
amine in mice. Nihon Hoigaku Zasshi. Jpn J Leg Med 1992;46(2):126-31.
188.
Yamamoto Y, Yamamoto K, Abiru H, et al. Effects of methamphetamine on rat
embryos cultured in vitro. Biol Neonate 1995;68(1):33-8.
189.
Mecham N, Melini J. Unintentional victims: development of a protocol for the care
of children exposed to chemicals at methamphetamine laboratories. Pediatr Emerg
Care 2002;18(4):327-32.
190.
Kolecki P. Inadvertent methamphetamine poisoning in pediatric patients. Pediatr
Emerg Care 1998;14(6):385-7.
191.
Matteucci MJ, Auten JD, Crowley B, et al. Methamphetamine exposures in young
children. Pediatr Emerg Care 2007;23(9):638-40.
192.
Gospe Jr. SM Transient cortical blindness in an infant exposed to methamphet-
amine. Ann Emerg Med 1995;26(3):380-2.
193.
Nagorka AR, Bergeson PS. Infant methamphetamine toxicity posing as scorpion
envenomation. Pediatr Emerg Care 1998;14(5):350-1.
194.
Logan BK, Fligner CL, Haddix T. Cause and manner of death in fatalities involving
methamphetamine. J Forensic Sci 1998;43(1):28-34.
195.
Inoue H, Ikeda N, Kudo K, et al. Methamphetamine-related sudden death with a
concentration which was of a “toxic level”. Leg Med 2006;8(3):150-5.
196.
Shaw KP. Human methamphetamine-related fatalities in Taiwan during 1991-1996.
J Forensic Sci 1999;44(1):27-31.
197.
Bailey DN, Shaw RF. Cocaine- and Methamphetamine-Related Deaths in San
Diego County, 1987: homicides and accidental overdoses. Forensic J 1989;34
(2):407-22.
198.
Katsumata S, Sato K, Kashiwade H, et al. Sudden death due presumably to internal
use of methamphetamine. Forensic Sci Int 1993;62(3):209-15.
199.
Chan P, Chen JH, Lee MH, et al. Fatal and nonfatal methamphetamine intoxication
in the intensive care unit. J Toxicol Clin Toxicol 1994;32(2):147-55.
200.
Ago M, Ago K, Hara K, et al. Toxicological and histopathological analysis of a
patient who died nine days after a single intravenous dose of methamphetamine: a
case report. Leg Med 2006;8(4):235-9.
DM, February 2012
85
201.
Takekawa K, Ohmori T, Kido A, et al. Methamphetamine body packer: acute
poisoning death due to massive leaking of methamphetamine. J Forensic Sci
2007;52(5):1219-22.
202.
Logan BK, Weiss EL, Harruff RC. Case report: distribution of methamphetamine
in a massive fatal ingestion. J Forensic Sci 1996;41(2):322-3.
203.
Sribanditmongkol P, Chokjamsai M, Thampitak S. Methamphetamine overdose
and fatality: 2 cases report. J Med Assoc Thai 2000;83(9):1120-3.
204.
Ishigami A, Kubo S-i, Gotohda T, et al. The application of immunohistochemical
findings in the diagnosis in methamphetamine-related death-two forensic autopsy
cases. J Med Invest 2003;50(1-2):112-6.
205.
Yamamoto K, Watanabe H, Ukita K, et al. [3 fatalities after communal use of
methamphetamine]. Arch Kriminol 1991;188(3-4):72-6.
206.
Logan BK. Methamphetamine and driving impairment. J Forensic Sci 1996;
41(3):457-64.
207.
Gustavsen I, Mørland J, Bramness JG. Impairment related to blood amphetamine
and/or methamphetamine concentrations in suspected drugged drivers. Accid Anal
Prev 2006;38(3):490-5.
208.
Schwilke EW, Sampaio dos Santos MI, Logan BK. Changing patterns of drug and
alcohol use in fatally injured drivers in Washington State. J Forensic Sci
2006;51(5):1191-8.
209.
Allcott 3rd, JV, Barnhart RA, Mooney LA. Acute lead poisoning in two users of
illicit methamphetamine. JAMA 1987;258(4):510-1.
210.
Centers for Disease Control and Prevention. Lead poisoning associated with
intravenous-methamphetamine use—Oregon, 1988. MMWR Morb Mortal Wkly
Repr 1989;38(48):830-1.
211.
Norton RL, Burton BT, McGirr J. Blood lead of intravenous drug users. J Toxicol
Clin Toxicol 1996;34(4):425-30.
212.
State Estimates of Past Year methamphetamine Use, SAMHSA Office of Applied
Studies. In: Substance Abuse Mental Health Services Administration, 2006;
Available from:
http://www.oas.samhsa.gov/2k6/stateMeth/stateMeth.htm.
213.
Methamphetamine Use, Abuse, and Dependence 2002, 2003, and 2004. 2005;
Available from:
http://www.oas.samhsa.gov/2k5/meth/meth.htm.
214.
Methamphetamine Use. Substance Abuse and Mental Health Services Administra-
tion, 2007; Available from:
http://www.oas.samhsa.gov/2k7/meth/meth.htm.
215.
Roberts DL. Amphetamine and Methamphetamine Emergency Department Visits,
1995-2002. The DAWN Report 2004 July 2004 [cited August 2011]; Available
from:
http://oas.samhsa.gov/2k4amphetamines.pdf.
216.
Emergency Department Visits Involving Methamphetamine, 2004-08, 2010 [up-
dated
August
24,
2010];
Available
from:
http://www.oas.samhsa.gov/
2k10/DAWN017/MethHTML.pdf.
217.
Freese TE, Obert J, Dickow A, et al. Methamphetamine abuse: Issue for special
populations. J Psychoact Drugs 2000;32(2):177.
218.
Centers for Disease Control and Prevention.
HIV/AIDS among men who have sex
with men, revised June 2007 [cited November 7, 2011]; Available from:
http://
img.thebody.com/cdc/2007/msm.pdf.
219.
DEA, Maps of Methamphetamine Lab Incidents. United States Drug Enforcement
Administration; 2011 [cited 2011, 2011]; Available from:
http://www.justice.gov/
dea/concern/map_lab_seizures.html.
86
DM, February 2012
220.
United Nations Office on Drugs and Crime. World Drug Report 2011. [cited
November 7, 2011]; Available from:
http://www.unodc.org/documents/data-
and-analysis/WDR2011/World_Drug_Report_2011_ebook.pdf.
221.
Burgess JL, Barnhart S, Checkoway H. Investigating clandestine drug laboratories:
adverse medical effects in law enforcement personnel. Am J Ind Med 1996;
30:488-94.
222.
Burgess J, Chandler D. Clandestine drug laboratories. In: Greenberg M, Hamilton
RJ, Phillips SD, and McCluskey GJ, eds. Occupational, Industrial, and Environ-
mental Toxicology. 2nd edn. Philadelphia, PA: Mosby, 2003. p. 746-65.
223.
Frank RS. The clandestine drug laboratory situation in the United States. J Forensic
Sci 1983;28(1):18-31.
224.
Allen A, Cantrell T. Synthetic reductions in clandestine amphetamine and meth-
amphetamine laboratories: a review. Forensic Sci Int 1989;42:183-99.
225.
Anglin M, Burke D, Perrochet B, et al. History of the methamphetamine problem.
J Psychoact Drugs 2000;32(2):137-41.
226.
Baker W, Antia U. A study of the use of ephedra in the manufacture of
methamphetamine. Forensic Sci Int 2007;1666:102-9.
227.
Skinner H. Methamphetamine synthesis via HI/red phosphorous reduction of
ephedrine. Forensic Sci Int 1990;48:128-34.
228.
Sexton R, Carlson R, Leukefeld C, et al. Patterns of Illicit methamphetamine
productions (“Cooking”) and associated risks in the rural south: an ethnographic
exploration. J Drug Issues 2006;Fall:853-76.
229.
New meth formula avoids anti-drug laws. Assoc Press 2009 [updated 8/24/20098/
3/2011]; Available from:
http://www.msnbc.msn.com/id/32542373/ns/us_news-
crime_and_courts/t/new-meth-formula-avoids-anti-drug-laws/-.TjluC830xaY.
230.
Blostein PA, Plaisier BR, Maltz SB, et al. Methamphetamine production is
hazardous to your health. J Trauma 2009;66:1712-7.
231.
Miller M, Kozel N. Methamphetamine abuse: epidemiologic issues and implica-
tions. Nida Res Monogr Ser 1991;115.
232.
Burke BA, Lewis RW, Latenser BA, et al. Methamphetamine-related burns in the
cornbelt. J Burn Care Res 2008;29:574-9.
233.
Santos AP, Wilson AK, Hornung CA, et al. Methamphetamine laboratory
explosions: a new and emerging burn injury. J Burn Care Rehabil 2005;26:228-32.
234.
Spann MD, McGwin G Jr, Kerby JD, et al. Characteristics of burn patients
injured in methamphetamine laboratory explosions. J Burn Care Res
2006;27:496-501.
235.
Warner P, Connolly JP, Gibran NS, et al. The methamphetamine burn patient.
J Burn Care Rehabil 2003;24:275-8.
236.
Charukamnoetkanok P, Wagoner MD. Facial and ocular injuries associated with
methamphetamine production accidents. Am J Ophthalmol 2004;138(5):875.
237.
Danks RR, Wibbenmeyer LA, Faucher LD, et al. Methamphetamine-associated
burn injuries: a retrospective analysis. J Burn Care Rehabil 2004;25:425-9.
238.
Arant T, Henry C, Clifford W, et al. Anhydrous ammonia thefts and releases
associated with illicit methamphetamine production—16 states, January 2000-June
2004. MMWR Morb Mortal Wkly Rep 2005;54(14):359-61.
239.
Bloom GR, Suhail F, Hopkins-Price P, et al. Acute anhydrous ammonia injury from
accidents during illicit methamphetamine production. Burns 2008;34(5):713-8.
DM, February 2012
87
240.
Martyny J, Arbuckle S, McCammon C Jr, et al. Chemical concentrations and
contamination associated with clandestine methamphetamine laboratories. J Chem
Health Saf 2007;14(4):40-52.
241.
Martyny J, Arbuckle S, McCammon C, et al. Chemical exposures associated with
clandestine methamphetamine laboratories using the anhydrous ammonia method
of production, 2004; Available from:
http://www.nationaljewish.org/about/
mediacenter/pressreleases/y2005/meth_research_results.aspx.
242.
White CE, Park MS, Renz EM, et al. burn center treatment of patients with severe
anhydrous ammonia injury: case reports and literature review. J Burn Care Res
2007;28(6):922-8.
243.
Amshel CE, Fealk MH, Phillips BJ, et al. Anhydrous ammonia burns case report
and review of the literature. Burns 2000;26(5):493-7.
244.
Willers-Russo LJ. Three fatalities involving phosphine gas, produced as a result of
methamphetamine manufacturing. J Forensic Sci 1999;44(3):647-52.
245.
Borak J, Diller WF. Phosgene exposure: mechanisms of injury and treatment
strategies. J Occup Environ Med 2001;43(2):110-9.
246.
Evison D, Hinsley D, Rice P. Chemical weapons. BMJ 2002;324(7333):332-5.
247.
Martyny J, Van Dyke M, McCammon C, et al. SL A. In: Chemical exposures
associated with clandestine methamphetamine laboratories using the hypophospho-
rous and phosphorous flake method of production, 2005; Available from:
http://
www.nationaljewish.org/about/mediacenter/pressreleases/y2005/meth_research_
results.aspx.
248.
Burgess J. Phosphine Exposure from a methamphetamine laboratory investigation.
Clin Toxicol 2001;39(2):165-8.
249.
Martyny J, Arbuckle S, McCammon JrC , et al. Chemical exposures associated with
clandestine methamphetamine laboratories, 2004; Available from:
http://www.
nationaljewish.org/about/mediacenter/pressreleases/y2005/meth_research_results.
aspx.
250.
VanDyke M, Erb N, Arbuckle S, et al. A 24-hour study to investigate persistent
chemical exposures associated with clandestine methamphetamine laboratories. J
Occup Environ Hyg 2009;6(2):82-9.
251.
Anonymous. Public health consequences among first responders to emergency
events associated with illicit methamphetamine laboratories - selected states,
1996-1999. MMWR Morb Mortal Wkly Rep 2000;49(45):1021-4.
252.
Manning T. Drug labs and endangered children. FBI Law Enforcement Bulletin
1999;68(7):10-4.
253.
Caldicott DG, Pigou PE, Beattie R, et al. Clandestine drug laboratories in Australia
and the Potential for Harm. Aust NZ J Public Health 2005;29(2):155-62.
254.
Mecham N, Melini J. Unintentional victims: development of a protocol for the care
of children exposed to chemicals at methamphetamine laboratories. Pediatr Emerg
Care 2002;18(4):327-32.
255.
Connell-Carrick K. Methamphetamine and changing face of child welfare: practice
principles of child welfare workers. Child Welf 2007;86(3):125-44.
256.
Farst K, Duncan JM, Moss M, et al. Methamphetamine exposure presenting as
caustic ingestions in children. Ann Emerg Med 2007;49:341-3.
257.
Kolecki P. Inadvertent methamphetamine poisoning in pediatric patients. Pediatr
Emerg Care 1998;14:385-7.
88
DM, February 2012
258.
Scott MS, Dedel K. Clandestine Methamphetamine Labs 2nd edition. US Depart-
ment of Justice Office of Community Oriented Policing Services 2006; [cited
November 7, 2011]; Available from:
http://www.cops.usdoj.gov/files/ric/Publications/
e07063402.pdf.
259.
Grant P. Evaluation of children removed from a clandestine methamphetamine
laboratory. Pediatr Emerg Med 2006;7:170-80.
260.
Hohman M, Oliver R, Wright W. Methamphetamine abuse and manufacture: the
child welfare response. Soc Work 2004;49(3):373-81.
261.
McGuinness TM, Pollack D. Parental methamphetamine abuse and children.
J Pediatr Health Care 2008;22:152-8.
262.
Messina N, Marinelli-Casey P, West K, et al. Children exposed to methamphet-
amine use and manufacture. Child Abus Negl 2007 [Epub ahead of print: Published
online 2007 March 22].
263.
Hammon TL, Griffin S. Support for selection of a methamphetamine cleanup
standard in colorado. Regul Toxicol Pharmacol 2007;48(1):102-14.
264.
Vandeveld N. Clandestine methamphetamine labs in Wisconsin. J Environ Health
2004;66(7):46-51.
265.
Guidelines for Law Enforcement for the Cleanup of Clandestine Drug Laboratories,
2005; Available from:
http://www.justice.gov/dea/resources/redbook.pdf.
266.
Hargreaves G. Clandestine drug labs chemical time bombs. FBI Law Enforcement
Bulletin 2000;69(4):1-6.
DM, February 2012
89
Document Outline




